������λ����������ҽԺ���ơ�����һԺ���ơ���������ҽԺ����ˮ̶ҽԺ����
NIPT�ٴ���������½�չ
���ߣ�Linlin ��λ�� ��Դ���й����������� ���ߣ�
�����������
2013-7-19 �Ķ�
�ֺţ�T|T
�������ٴ������о�
̥��Ⱦɫ����������쳣������ǰ��⣨NIPT����������һ����ͨ���������ķ�չ���������о���Ա�����˴������ٴ������һ��̽�ָü����ڲ�ǰ����е�Ӧ�á�
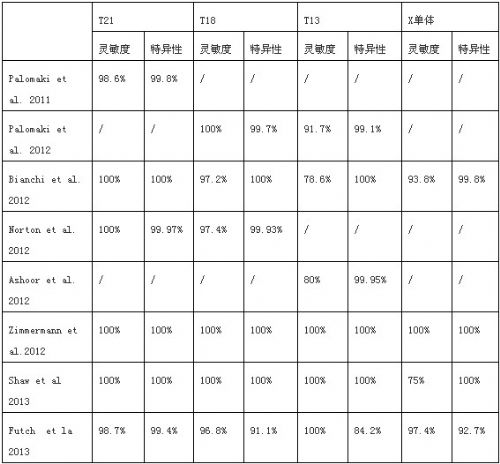
2008����������ͬ�ĺ����о�С��(Chiu����. 2008; Fan����. 2008)���ô��ģƽ�в�������MPS��������21�����ۺ���̥�����и�������Ѫ�з����˳�����21��Ⱦɫ�塣�������̷��������ٴ����飬�ٴ���֤�˴��ģƽ�в���MPS����Ⱦɫ���������ļ�����и������Ⱥ������ԣ�����1�������ǣ���2011�����ʼ��������ǰ�ٴ��翪ʼ����NIPT�Ը�Σ�и����м�⡣Palomaki���ˣ�2011�����о���֤��MPS�Ը�Σ����ĸ��Ѫ��̥��T21�ļ��ӵ�н�99���������Ⱥ������ԣ����ﶨ���Σ�������ذ����������䡢���岡ʷ��Ѫ��ѧɸ���Σ�ͳ���ɸ���Σ������С�飨Palomaki�ȣ�2012�����ַ���һ���о���ʾMPS��T18����������Ϊ100������������Ϊ0.28������T13����������Ϊ91.7������������Ϊ0.97�������T13��T18��T21���ĸ���������Ϊ98.9�������ϼ�������Ϊ1.4����Bianchi���ˣ�2012��Ҳ����MPS�Ը�Σ�����и���Ѫ����м�⣬���㷨�������в�ͬ���������о��У�NIPT���T21��T18��T13���������ȷֱ�Ϊ100����97.2����78.6���������Խ�Ϊ100�������ǻ�������NIPTҲ�ܼ�������Ⱦɫ��������壬Ҳ������λ�������Լ�Ƕ�������塣�ر��ǣ���XȾɫ�嵥�����������Ϊ93.8����������Ϊ99.8�������⣬Bianchi����ͬʱ��ΪNIPT�ڲ��õĽ���Ҳ�ɶ�����Ⱦɫ���쳣����ɸ�顣Mazloom���˺ܿ�ͽ�һ��֤ʵ����һ�۵㣬�����ڻ���MPS�����Ļ����ϣ�ͨ�����������Ⱦɫ��ķ����㷨������[47,XXX], [45,X], [47,XXY], and [47,XYY]���ڵļ�����Ⱦɫ���ۺ������м�⣬�����ĸ���������Ϊ96.2%��������Ϊ0.3%����һ�����ʾ����⼼���������ۺ�����XYY�������ۺ�֢�ĵļ�⾫ȷ�Ƚӽ���Ⱦɫ�壬���Կ��ǽ���Ӧ�����ٴ���
����һЩ�о���Ա����ѡ���Ե�Ⱦɫ������������÷����Ƕ�ĸ��Ѫ������DNA���ض���Ⱦɫ��������в���Sparks���ˣ�2012�������������һ������ĺ������ٴ��о�����Խ���CVS����ˮ���������и���Ⱥ������Ⱦɫ��ѡ���ԵIJ�����T21��T18���м�⡣��Norton�ȣ�2012��������1��������ѡ���������ֻ�������DANSR�������Լ�FORTE�㷨���з���������Ԥ��cut-offֵΪ1�����и߷�����ͷ��յĽ綨�������ʾ��T21����������Ⱥ������Էֱ�Ϊ100����99.97���� T18�������Ⱥ������Էֱ�Ϊ97.4����99.93��������ַ�����һƪ���£�Ashoor���ˣ�2012������ʹ��DANSR��FORTE������һ��ع��ԵIJ��������о��У���T13���������Ⱥ������Էֱ�Ϊ80����99.95����Zimmermann��2012��ͨ����166��������Ⱦɫ���̬��λ�����ѡ���ԵIJ����������ʹ��MATLAB (MathWorks, Natick, MA, USA) ʵ�����ṩͳ�ļ��㷽����Ⱦɫ�忽�������з�����㣬�临�ϼ��㾫�ȴﵽ��99.8%����һ��45X��DNA��������û�ܼ��������19��Ⱦɫ���������ﵽ��100%�������Ⱥ������ԡ���Щ�о�֤ʵNIPT�ڸ߷����и���Ⱥ�У����T21��T13��T18�ļ����һ�ֿɿ��ķ�����
ͬ����Ը����������Ҳ���������ڴ��ģ�ٴ����顣���������ˣ�2013����һ��412����Ч�����Ļع����ٴ����飬��������ۺ�����Σ�и�����MPS����NIPT��⣬�����ʾ��T21��T18��T13���ϼ��������Ϊ100%�����ϼ�������Ը���99.7%��ͬʱ�����Ҳӡ֤��ͨ��һ�μ���ͬʱ��ȫ��Ⱦɫ�����������й۲졣����һ������ģ��ǰհ�Ե��ٴ������ռ��˳���2000���и�Ѫ����������ȣ�2013����ͬ������MPS��T21��T18��T13���м�⣬�����Ϊ100%����������Ϊ0.05%�������о��е���35��ķǸ����и�����Ѫ��ѧɸ������Ϊ���գ�����֤ʵNIPTӵ��Զ���ڴ�ͳѪ��ѧɸ��������Ⱥ������ԣ�����һ����֤NIPTδ�����еȷ��ռ��ͷ����и���Ⱥ��Ӧ�á�����̨���һ������ĺ����о���ʾ��Shaw�ȣ�2013������100������Σ�и�Ⱥ���У���һ��45X����DNA��������δ��ʶ���⣬����Ⱦɫ���������ȫ����������ϼ���ʳ�Ϊ96.4%�����Ե�Σ��Ⱥ��201������δ����Ⱦɫ���쳣�����֤ʵ������Ϊ100%����ı���͵��ǣ������о�Ҳ����NIPT���еȷ�����Ⱥ��Ӧ�þ������Ƶ������Ⱥ������ԣ�Nicolaides���ˣ�2012������Ԥʾ������Խ��Խ���ٴ����ݵĻ��ۣ�δ��NIPT���Ը��ǵ��еȷ����и���Ⱥ��Norton�ȣ�2012����
����NIPT ���ٴ��Ĵ��ģʵ������ѧС��չ����Խ��Խ��ϸ��������о���Futch(2013��)��������ܽ���2012��2��-7�¼�5974���ٴ������ļ����������1�������Կ���Ӱ��������������������������ۣ��о���Ϊ��̥��Ƕ�ϣ�ĸ��Ķ���������ĸ��Ƕ���壬˫��̥��һ̥ͣ���������Ӧ���ǵ����������Ĺ��̵��У���������һ������ǰ�����ٴ����ܲ��������⣬���ܺ�DNA��ĸѪ�еİٷֺ���Ҳ��Ӱ����������Ҫ���أ�Wang���ˣ�2013����22,384�������������֣�ĸѪ����̥��DNA�������и����سɷ��ȣ������ܳ����ȣ���10-21���ܼ䣬̥��DNA����ÿ������0.1%������21����ʱ��DNA����ÿ������1%���ڳ��β�ѪDNA�������������£�ƽ��3.6�ܺ��ٴβ�Ѫ��DNA�������ձ���ߡ�
��������⼼���IJ��Ϸ�չ���������ڳ���ͨ��MPS������Ⱦɫ��ṹ�쳣���м�⣬Srinivasan��2013����11������������ϵ�̥������DNA�����˷�������ÿ�����������˴�Լ109��25���Ŀ��Ƭ�εIJ��������ͨ�������м����һ��������������Ƕ�����⣬MPS������ȫ����7��ȱʧ���ظ�����λ��20��Ⱦɫ�����塣�����������ں��ͷ��������ڵı���Ҳ��Ϊ(Lau��2013)��ͨ��������Ϣѧ�����IJ��ϸĽ�������MPS������̥��Ⱦɫ��ṹ�쳣���м����п����ԡ�����Ԥ��������ǰ����ڲ��õĽ������и�Ϊ�㷺���ٴ���;��{NextPage}
��1. NIPT���Ĵ��ٴ�����������Ⱥ�������
������ָ�����/ר�ҹ�ʶ
��Ȼ�������ٴ��о���ʮ�ֹ㷺�Ŀ�չ��������Ϊֹ��רҵЭ�Ṳʶ�����NIPT��ָ�������Ϊ�����ࡣ2012��ISPD������������ǡ�����Ŵ���ѯ�����£�ͨ������ɸ�鷽����ĸ���������岡ʷȷ��Ϊ�߷��յ��и������Խ���NIPT��benn�ȡ�2012A����ͬ������������ѧ�ᣨACOG��������ĸ̥ҽѧ�ᣨSMFM��Ҳ��ͬ����ίԱ��ָ��������Ƽ���DNA��ǰ�����Ϊ���������Σ��Ⱥ��һ�ֳ�ɸ��⡣ѧ��ͬʱ��ϸ�綨�˷��������Σ��Ⱥ��1��ĸ�����䳬��35�ꣻ2�����������ʾ���������Σ��3�����������廼����4�������ڣ������ڻ�����ɸ�顢����ɸ����ַ����������Խ����5����ĸΪ��ѷ��λ��
���NIPTѸ�ͷ�չ�����ٴ��Ŵ���ѯ���������⣬2013��1�����������Ŵ���ѯʦЭ�ᣨNSGC�������DNA��ǰ�����Ŵ���ѯ����ָ�������NSGC��Ϊ
1��NIPT��ǰֻ��Ϊ��ǰȾɫ��������������IJ����⣬����������Ϊ��ϣ��쳣�������ͨ���д������ȷ�2����ȱ�����еͷ�����Ⱥ�е��ٴ�����NIPT��ʱ����������е�Ⱦɫ�������ɸ�鷽����3�����е��ٴ�������ʾNIPTֻ�ܺ���T21��T18��T13�ȣ��������и����֮ǰӦ����˵��������ļ�ⷶΧ�;����ԣ�4�������Ӽ��ǰ�ͼ�����Ŵ���ѯ����������ȷ����ѯ�����5�������������쳣��������Ⱦɫ���쳣��ʷ�����������������䡢ɸ�����Եȣ�������NIPT�����Σ���Ӧ���������ϸ���Ŵ���ѯ��6��NIPT��չѸ�٣��ٴ����������ݱ��NSGCҲ������NIPT�ķ�չ�����Ŵ���ѯ��ָ�������
2013��4�£�ISPD�ٴη���ָ�������Benn�ȣ�2013�����ڴ�ǰ�Ļ����Ͻ�����µĽ�չ����ֵ����⣬���һЩ�¹۵㡣NIPT����Ⱦɫ���ɸ���ʽϵͣ�������˫̥һ̥��������ʱ���������ȷ������Ƕ���壨����������̥��Ƕ���壩���������ȷ��������ͬ��4�£�����ҽѧ�Ŵ�ѧ��������ѧѧ�ᣨACMG���ڿ϶�NIPT���ߵ�ȷ�ʺͽϵ͵ļ������ʵ�ͬʱ��Ҳ���NIPT�ľ����ԡ��Ŵ���ѯ���ٴ�������������
����������ȫ����ǰ��ϼ���ר����Ҳ��2012�����DNA��ǰ��⼼����������֤�����������ˡ�2012����ָ���ü�⼼����һ�֡����������ˮƽ������Ŀ�꼲��ָ��ȷ���IJ�ǰ��ɸ���¼�����Ӧ�������еIJ�ǰɸ����ϵ���ϣ���ȷ�����ٴ�������Ⱥ������1���н����Բ�ǰ��Ͻ���֢�ߣ��������������ȡ��г�Ѫ����Ⱦδ���ȣ���2�� ��ǰɸ���Σ���ٽ��Σ�и������������1/270-1/1000����3�� ������֪���ܾ������Բ�ǰ��ϵ��и���4���Խ����Բ�ǰ��ϼ��Ƚ��ǵ��и���5������ʱ���ڽϴ����ܳ���Ŀǰ��ǰɸ�鷶Χ���и���
����� ACMG statement on noninvasive prenatal screening for fetal aneuploidy. Genet Med. 2013 May;15(5):395-8.
Benn, P., Borrell, A., Cuckle, H., Dugoff, L., Gross, S., Johnson, J. A.,et al. (2012a). Prenatal Detection of Down Syndrome using Massively Parallel Sequencing (MPS): a rapid response statement from a committee on behalf of the Board of the International Society for Prenatal Diagnosis, 24 October 2011. Prenatal Diagnosis, 32(1), 1�C2. doi:10.1002/pd.2919. Benn, P., Cuckle, H., & Pergament, E. (2012b). Non-invasive prenatal diagnosis for Down syndrome: the paradigm will shift, but slowly. Ultrasound in Obstetrics & Gynecology, 39(2), 127�C130. doi:10.1002/uog.11083.
Benn P, Borell A,et al. Position statement from the Aneuploidy Screening Committee on behalf of the Board of the International Society for Prenatal Diagnosis. Prenat Diagn. 2013 Apr 24:1-8.
�������������֣�����쿣�2012������ǰ��ϣ����й��Լ��ĵ�·���л���������־��47��801-803 Bianchi, D. W., Platt, L. D., Goldberg, J. D., Abuhamad, A. Z., Sehnert, A. J., & Rava, R. P. (2012). Genome-Wide Fetal Aneuploidy Detection by Maternal Plasma DNA Sequencing. Obstetrics and Gynecology, 119(5), 1�C13.
Chan, K., Yam, I., Leung, K. Y., Tang, M., Chan, T. K., & Chan, V.(2010). Detection of paternal alleles in maternal plasma for noninvasive prenatal diagnosis of beta-thalassemia: a feasibility study in southern Chinese. European Journal of Obstetrics, Gynecology, and Reproductive Biology, 150(1), 28�C33.
Chiu, R. W., Chan, K. C., Gao, Y., Lau, V. Y., Zheng, W., Leung, T. Y., et al. (2008). Noninvasive prenatal diagnosis of fetal chromosomal aneuploidy by massively parallel genomic sequencing of DNA in maternal plasma. Proceedings of the National Academy of Sciences of the United States of America, 105(51), 20458�C20463. Fan, H. C., Blumenfeld, Y. J., Chitkara, U., Hudgins, L., & Quake, S.R. (2008). Noninvasive diagnosis of fetal aneuploidy by shotgun sequencing DNA from maternal blood. Proceedings of the National Academy of Sciences of the United States of America, 105(42), 16266�C16271. Futch, T., Spinosa,J., et al.(2013) Initial clinical laboratory experience in noninvasive prenatal testing for fetal aneuploidy from maternal plasma DNA samples. Prenatal Diagnosis , 33, 569�C574
Lau, T.K., Jiang, F.M., et al, Secondary findings from non-invasive prenatal testing for common fetal aneuploidies by whole genome sequencing as a clinical service Prenatal Diagnosis 2013, 33, 1�C7 Liang, D.S., Lv, W. G., Wang, H., Xu, L.P., et al.(2012) Non-invasive prenatal testing of fetal whole chromosome aneuploidy by massively parallel sequencing. Prenatal Diagnosis, 32,1-7
Lo, Y. M., Corbetta, N., Chamberlain, P. F., Rai, V., Sargent, I. L.,Redman, C. W., et al. (1997). Presence of fetal DNA in maternal plasma and serum. Lancet, 350(9076), 485�C487. Mazloom,A.R., D?akula,Z., et al. Noninvasive Prenatal Detection of Sex Chromosomal Aneuploidies by Sequencing Circulating Cell-Free DNA from Maternal Plasma Nicolaides, K. H., Syngelaki, A., Ashoor, G., Birdir, C., & Touzet, G. (2012). Noninvasive prenatal testing for fetal trisomies in a routinely screened first-trimester population. American Journal of Obstetrics and Gynecology, 207, x.ex�Cx.ex. Norton, M. E., Brar, H., Weiss, J., Karimi, A., Laurent, L. C., Caughey, A. B., et al. (2012). Non-Invasive Chromosomal Evaluation (NICE) study: results of a multicenter, prospective, Cohort study for detection of fetal trisomy 21 and trisomy 18. American Journal of Obstetrics and Gynecology, 207(2), 137.e1�C8. Epub 2012 Jun 1.
NSGC (2010). NSGC Position Statement: Reproductive Freedom. Retrieved from http://www.nsgc.org/Media/PositionStatements/tabid/330/Default.aspx Palomaki, G. E., Kloza, E. M., Lambert-Messerlian, G. M., Haddow, J. E., Neveux, L. M., Ehrich, M., et al. (2011). DNA sequencing of maternal plasma to detect Down syndrome: an international clinical validation study. Genetics in Medicine, 13(11), 913�C920.
Palomaki, G. E., Deciu, C., Kloza, E. M., Lambert-Messerlian, G. M., Haddow, J. E., Neveux, L. M., et al. (2012). DNA sequencing of maternal plasma reliably identifies trisomy 18 and trisomy 13 as well as Down syndrome: an international collaborative study. Genetics in Medicine, 14(3), 296�C305. doi:10.1038/gim.2011.73. Srinivasan,A.,Bianchi.D.W., et alNoninvasive Detection of Fetal Subchromosome Abnormalities via Deep Sequencing of Maternal Plasma. The American Journal of Human Genetics 92, 1�C10, February 7, 2013
Shaw, S.W. Steven, Hsiao,ching Hua, Chen, Chih-yao, et al.,Noninvasive prenatal testing for whole fetal chromosomal aneuploidies: A multicentre prospective cohort trial in Taiwan, Prenatal Diagnosis Song,Y.J., Liu,C.C., Qi,H., et al,(2013) Non invasive prenatal testing of fetal aneuploidies by massively parallel sequencing in a prospective chinese population. Accepted for Prenatal Diagnosis Sparks, A. B., Struble, C. A., Wang, E. T., Song, K., & Oliphant, A. (2012). Noninvasive prenatal detection and selective analysis of cell-free DNA obtained from maternal blood: evaluation for trisomy 21 and trisomy 18. American Journal of Obstetrics and Gynecology, 206(4), 319.e1�C9. Epub 2012 Jan 26.
Wang E, Batey A, Struble C, Musci T, Song K, Oliphant A ,Gestational Age and Maternal Weight Effects on Fetal cfDNA in Maternal Plasma Prenat Diagn. 2013 Apr 2:1-5. Zimmermann,B., Hill,m., et al, Noninvasive prenatal aneuploidy testing of chromosomes 13, 18,21, X, and Y, using targeted sequencing of polymorphic loci. Prenatal Diagnosis 2012, 32, 1�C9
̥��Ⱦɫ����������쳣������ǰ��⣨NIPT����������һ����ͨ���������ķ�չ���������о���Ա�����˴������ٴ������һ��̽�ָü����ڲ�ǰ����е�Ӧ�á�
2008����������ͬ�ĺ����о�С��(Chiu����. 2008; Fan����. 2008)���ô��ģƽ�в�������MPS��������21�����ۺ���̥�����и�������Ѫ�з����˳�����21��Ⱦɫ�塣�������̷��������ٴ����飬�ٴ���֤�˴��ģƽ�в���MPS����Ⱦɫ���������ļ�����и������Ⱥ������ԣ�����1�������ǣ���2011�����ʼ��������ǰ�ٴ��翪ʼ����NIPT�Ը�Σ�и����м�⡣Palomaki���ˣ�2011�����о���֤��MPS�Ը�Σ����ĸ��Ѫ��̥��T21�ļ��ӵ�н�99���������Ⱥ������ԣ����ﶨ���Σ�������ذ����������䡢���岡ʷ��Ѫ��ѧɸ���Σ�ͳ���ɸ���Σ������С�飨Palomaki�ȣ�2012�����ַ���һ���о���ʾMPS��T18����������Ϊ100������������Ϊ0.28������T13����������Ϊ91.7������������Ϊ0.97�������T13��T18��T21���ĸ���������Ϊ98.9�������ϼ�������Ϊ1.4����Bianchi���ˣ�2012��Ҳ����MPS�Ը�Σ�����и���Ѫ����м�⣬���㷨�������в�ͬ���������о��У�NIPT���T21��T18��T13���������ȷֱ�Ϊ100����97.2����78.6���������Խ�Ϊ100�������ǻ�������NIPTҲ�ܼ�������Ⱦɫ��������壬Ҳ������λ�������Լ�Ƕ�������塣�ر��ǣ���XȾɫ�嵥�����������Ϊ93.8����������Ϊ99.8�������⣬Bianchi����ͬʱ��ΪNIPT�ڲ��õĽ���Ҳ�ɶ�����Ⱦɫ���쳣����ɸ�顣Mazloom���˺ܿ�ͽ�һ��֤ʵ����һ�۵㣬�����ڻ���MPS�����Ļ����ϣ�ͨ�����������Ⱦɫ��ķ����㷨������[47,XXX], [45,X], [47,XXY], and [47,XYY]���ڵļ�����Ⱦɫ���ۺ������м�⣬�����ĸ���������Ϊ96.2%��������Ϊ0.3%����һ�����ʾ����⼼���������ۺ�����XYY�������ۺ�֢�ĵļ�⾫ȷ�Ƚӽ���Ⱦɫ�壬���Կ��ǽ���Ӧ�����ٴ���
����һЩ�о���Ա����ѡ���Ե�Ⱦɫ������������÷����Ƕ�ĸ��Ѫ������DNA���ض���Ⱦɫ��������в���Sparks���ˣ�2012�������������һ������ĺ������ٴ��о�����Խ���CVS����ˮ���������и���Ⱥ������Ⱦɫ��ѡ���ԵIJ�����T21��T18���м�⡣��Norton�ȣ�2012��������1��������ѡ���������ֻ�������DANSR�������Լ�FORTE�㷨���з���������Ԥ��cut-offֵΪ1�����и߷�����ͷ��յĽ綨�������ʾ��T21����������Ⱥ������Էֱ�Ϊ100����99.97���� T18�������Ⱥ������Էֱ�Ϊ97.4����99.93��������ַ�����һƪ���£�Ashoor���ˣ�2012������ʹ��DANSR��FORTE������һ��ع��ԵIJ��������о��У���T13���������Ⱥ������Էֱ�Ϊ80����99.95����Zimmermann��2012��ͨ����166��������Ⱦɫ���̬��λ�����ѡ���ԵIJ����������ʹ��MATLAB (MathWorks, Natick, MA, USA) ʵ�����ṩͳ�ļ��㷽����Ⱦɫ�忽�������з�����㣬�临�ϼ��㾫�ȴﵽ��99.8%����һ��45X��DNA��������û�ܼ��������19��Ⱦɫ���������ﵽ��100%�������Ⱥ������ԡ���Щ�о�֤ʵNIPT�ڸ߷����и���Ⱥ�У����T21��T13��T18�ļ����һ�ֿɿ��ķ�����
ͬ����Ը����������Ҳ���������ڴ��ģ�ٴ����顣���������ˣ�2013����һ��412����Ч�����Ļع����ٴ����飬��������ۺ�����Σ�и�����MPS����NIPT��⣬�����ʾ��T21��T18��T13���ϼ��������Ϊ100%�����ϼ�������Ը���99.7%��ͬʱ�����Ҳӡ֤��ͨ��һ�μ���ͬʱ��ȫ��Ⱦɫ�����������й۲졣����һ������ģ��ǰհ�Ե��ٴ������ռ��˳���2000���и�Ѫ����������ȣ�2013����ͬ������MPS��T21��T18��T13���м�⣬�����Ϊ100%����������Ϊ0.05%�������о��е���35��ķǸ����и�����Ѫ��ѧɸ������Ϊ���գ�����֤ʵNIPTӵ��Զ���ڴ�ͳѪ��ѧɸ��������Ⱥ������ԣ�����һ����֤NIPTδ�����еȷ��ռ��ͷ����и���Ⱥ��Ӧ�á�����̨���һ������ĺ����о���ʾ��Shaw�ȣ�2013������100������Σ�и�Ⱥ���У���һ��45X����DNA��������δ��ʶ���⣬����Ⱦɫ���������ȫ����������ϼ���ʳ�Ϊ96.4%�����Ե�Σ��Ⱥ��201������δ����Ⱦɫ���쳣�����֤ʵ������Ϊ100%����ı���͵��ǣ������о�Ҳ����NIPT���еȷ�����Ⱥ��Ӧ�þ������Ƶ������Ⱥ������ԣ�Nicolaides���ˣ�2012������Ԥʾ������Խ��Խ���ٴ����ݵĻ��ۣ�δ��NIPT���Ը��ǵ��еȷ����и���Ⱥ��Norton�ȣ�2012����
����NIPT ���ٴ��Ĵ��ģʵ������ѧС��չ����Խ��Խ��ϸ��������о���Futch(2013��)��������ܽ���2012��2��-7�¼�5974���ٴ������ļ����������1�������Կ���Ӱ��������������������������ۣ��о���Ϊ��̥��Ƕ�ϣ�ĸ��Ķ���������ĸ��Ƕ���壬˫��̥��һ̥ͣ���������Ӧ���ǵ����������Ĺ��̵��У���������һ������ǰ�����ٴ����ܲ��������⣬���ܺ�DNA��ĸѪ�еİٷֺ���Ҳ��Ӱ����������Ҫ���أ�Wang���ˣ�2013����22,384�������������֣�ĸѪ����̥��DNA�������и����سɷ��ȣ������ܳ����ȣ���10-21���ܼ䣬̥��DNA����ÿ������0.1%������21����ʱ��DNA����ÿ������1%���ڳ��β�ѪDNA�������������£�ƽ��3.6�ܺ��ٴβ�Ѫ��DNA�������ձ���ߡ�
��������⼼���IJ��Ϸ�չ���������ڳ���ͨ��MPS������Ⱦɫ��ṹ�쳣���м�⣬Srinivasan��2013����11������������ϵ�̥������DNA�����˷�������ÿ�����������˴�Լ109��25���Ŀ��Ƭ�εIJ��������ͨ�������м����һ��������������Ƕ�����⣬MPS������ȫ����7��ȱʧ���ظ�����λ��20��Ⱦɫ�����塣�����������ں��ͷ��������ڵı���Ҳ��Ϊ(Lau��2013)��ͨ��������Ϣѧ�����IJ��ϸĽ�������MPS������̥��Ⱦɫ��ṹ�쳣���м����п����ԡ�����Ԥ��������ǰ����ڲ��õĽ������и�Ϊ�㷺���ٴ���;��{NextPage}
��1. NIPT���Ĵ��ٴ�����������Ⱥ�������

������ָ�����/ר�ҹ�ʶ
��Ȼ�������ٴ��о���ʮ�ֹ㷺�Ŀ�չ��������Ϊֹ��רҵЭ�Ṳʶ�����NIPT��ָ�������Ϊ�����ࡣ2012��ISPD������������ǡ�����Ŵ���ѯ�����£�ͨ������ɸ�鷽����ĸ���������岡ʷȷ��Ϊ�߷��յ��и������Խ���NIPT��benn�ȡ�2012A����ͬ������������ѧ�ᣨACOG��������ĸ̥ҽѧ�ᣨSMFM��Ҳ��ͬ����ίԱ��ָ��������Ƽ���DNA��ǰ�����Ϊ���������Σ��Ⱥ��һ�ֳ�ɸ��⡣ѧ��ͬʱ��ϸ�綨�˷��������Σ��Ⱥ��1��ĸ�����䳬��35�ꣻ2�����������ʾ���������Σ��3�����������廼����4�������ڣ������ڻ�����ɸ�顢����ɸ����ַ����������Խ����5����ĸΪ��ѷ��λ��
���NIPTѸ�ͷ�չ�����ٴ��Ŵ���ѯ���������⣬2013��1�����������Ŵ���ѯʦЭ�ᣨNSGC�������DNA��ǰ�����Ŵ���ѯ����ָ�������NSGC��Ϊ
1��NIPT��ǰֻ��Ϊ��ǰȾɫ��������������IJ����⣬����������Ϊ��ϣ��쳣�������ͨ���д������ȷ�2����ȱ�����еͷ�����Ⱥ�е��ٴ�����NIPT��ʱ����������е�Ⱦɫ�������ɸ�鷽����3�����е��ٴ�������ʾNIPTֻ�ܺ���T21��T18��T13�ȣ��������и����֮ǰӦ����˵��������ļ�ⷶΧ�;����ԣ�4�������Ӽ��ǰ�ͼ�����Ŵ���ѯ����������ȷ����ѯ�����5�������������쳣��������Ⱦɫ���쳣��ʷ�����������������䡢ɸ�����Եȣ�������NIPT�����Σ���Ӧ���������ϸ���Ŵ���ѯ��6��NIPT��չѸ�٣��ٴ����������ݱ��NSGCҲ������NIPT�ķ�չ�����Ŵ���ѯ��ָ�������
2013��4�£�ISPD�ٴη���ָ�������Benn�ȣ�2013�����ڴ�ǰ�Ļ����Ͻ�����µĽ�չ����ֵ����⣬���һЩ�¹۵㡣NIPT����Ⱦɫ���ɸ���ʽϵͣ�������˫̥һ̥��������ʱ���������ȷ������Ƕ���壨����������̥��Ƕ���壩���������ȷ��������ͬ��4�£�����ҽѧ�Ŵ�ѧ��������ѧѧ�ᣨACMG���ڿ϶�NIPT���ߵ�ȷ�ʺͽϵ͵ļ������ʵ�ͬʱ��Ҳ���NIPT�ľ����ԡ��Ŵ���ѯ���ٴ�������������
����������ȫ����ǰ��ϼ���ר����Ҳ��2012�����DNA��ǰ��⼼����������֤�����������ˡ�2012����ָ���ü�⼼����һ�֡����������ˮƽ������Ŀ�꼲��ָ��ȷ���IJ�ǰ��ɸ���¼�����Ӧ�������еIJ�ǰɸ����ϵ���ϣ���ȷ�����ٴ�������Ⱥ������1���н����Բ�ǰ��Ͻ���֢�ߣ��������������ȡ��г�Ѫ����Ⱦδ���ȣ���2�� ��ǰɸ���Σ���ٽ��Σ�и������������1/270-1/1000����3�� ������֪���ܾ������Բ�ǰ��ϵ��и���4���Խ����Բ�ǰ��ϼ��Ƚ��ǵ��и���5������ʱ���ڽϴ����ܳ���Ŀǰ��ǰɸ�鷶Χ���и���
����� ACMG statement on noninvasive prenatal screening for fetal aneuploidy. Genet Med. 2013 May;15(5):395-8.
Benn, P., Borrell, A., Cuckle, H., Dugoff, L., Gross, S., Johnson, J. A.,et al. (2012a). Prenatal Detection of Down Syndrome using Massively Parallel Sequencing (MPS): a rapid response statement from a committee on behalf of the Board of the International Society for Prenatal Diagnosis, 24 October 2011. Prenatal Diagnosis, 32(1), 1�C2. doi:10.1002/pd.2919. Benn, P., Cuckle, H., & Pergament, E. (2012b). Non-invasive prenatal diagnosis for Down syndrome: the paradigm will shift, but slowly. Ultrasound in Obstetrics & Gynecology, 39(2), 127�C130. doi:10.1002/uog.11083.
Benn P, Borell A,et al. Position statement from the Aneuploidy Screening Committee on behalf of the Board of the International Society for Prenatal Diagnosis. Prenat Diagn. 2013 Apr 24:1-8.
�������������֣�����쿣�2012������ǰ��ϣ����й��Լ��ĵ�·���л���������־��47��801-803 Bianchi, D. W., Platt, L. D., Goldberg, J. D., Abuhamad, A. Z., Sehnert, A. J., & Rava, R. P. (2012). Genome-Wide Fetal Aneuploidy Detection by Maternal Plasma DNA Sequencing. Obstetrics and Gynecology, 119(5), 1�C13.
Chan, K., Yam, I., Leung, K. Y., Tang, M., Chan, T. K., & Chan, V.(2010). Detection of paternal alleles in maternal plasma for noninvasive prenatal diagnosis of beta-thalassemia: a feasibility study in southern Chinese. European Journal of Obstetrics, Gynecology, and Reproductive Biology, 150(1), 28�C33.
Chiu, R. W., Chan, K. C., Gao, Y., Lau, V. Y., Zheng, W., Leung, T. Y., et al. (2008). Noninvasive prenatal diagnosis of fetal chromosomal aneuploidy by massively parallel genomic sequencing of DNA in maternal plasma. Proceedings of the National Academy of Sciences of the United States of America, 105(51), 20458�C20463. Fan, H. C., Blumenfeld, Y. J., Chitkara, U., Hudgins, L., & Quake, S.R. (2008). Noninvasive diagnosis of fetal aneuploidy by shotgun sequencing DNA from maternal blood. Proceedings of the National Academy of Sciences of the United States of America, 105(42), 16266�C16271. Futch, T., Spinosa,J., et al.(2013) Initial clinical laboratory experience in noninvasive prenatal testing for fetal aneuploidy from maternal plasma DNA samples. Prenatal Diagnosis , 33, 569�C574
Lau, T.K., Jiang, F.M., et al, Secondary findings from non-invasive prenatal testing for common fetal aneuploidies by whole genome sequencing as a clinical service Prenatal Diagnosis 2013, 33, 1�C7 Liang, D.S., Lv, W. G., Wang, H., Xu, L.P., et al.(2012) Non-invasive prenatal testing of fetal whole chromosome aneuploidy by massively parallel sequencing. Prenatal Diagnosis, 32,1-7
Lo, Y. M., Corbetta, N., Chamberlain, P. F., Rai, V., Sargent, I. L.,Redman, C. W., et al. (1997). Presence of fetal DNA in maternal plasma and serum. Lancet, 350(9076), 485�C487. Mazloom,A.R., D?akula,Z., et al. Noninvasive Prenatal Detection of Sex Chromosomal Aneuploidies by Sequencing Circulating Cell-Free DNA from Maternal Plasma Nicolaides, K. H., Syngelaki, A., Ashoor, G., Birdir, C., & Touzet, G. (2012). Noninvasive prenatal testing for fetal trisomies in a routinely screened first-trimester population. American Journal of Obstetrics and Gynecology, 207, x.ex�Cx.ex. Norton, M. E., Brar, H., Weiss, J., Karimi, A., Laurent, L. C., Caughey, A. B., et al. (2012). Non-Invasive Chromosomal Evaluation (NICE) study: results of a multicenter, prospective, Cohort study for detection of fetal trisomy 21 and trisomy 18. American Journal of Obstetrics and Gynecology, 207(2), 137.e1�C8. Epub 2012 Jun 1.
NSGC (2010). NSGC Position Statement: Reproductive Freedom. Retrieved from http://www.nsgc.org/Media/PositionStatements/tabid/330/Default.aspx Palomaki, G. E., Kloza, E. M., Lambert-Messerlian, G. M., Haddow, J. E., Neveux, L. M., Ehrich, M., et al. (2011). DNA sequencing of maternal plasma to detect Down syndrome: an international clinical validation study. Genetics in Medicine, 13(11), 913�C920.
Palomaki, G. E., Deciu, C., Kloza, E. M., Lambert-Messerlian, G. M., Haddow, J. E., Neveux, L. M., et al. (2012). DNA sequencing of maternal plasma reliably identifies trisomy 18 and trisomy 13 as well as Down syndrome: an international collaborative study. Genetics in Medicine, 14(3), 296�C305. doi:10.1038/gim.2011.73. Srinivasan,A.,Bianchi.D.W., et alNoninvasive Detection of Fetal Subchromosome Abnormalities via Deep Sequencing of Maternal Plasma. The American Journal of Human Genetics 92, 1�C10, February 7, 2013
Shaw, S.W. Steven, Hsiao,ching Hua, Chen, Chih-yao, et al.,Noninvasive prenatal testing for whole fetal chromosomal aneuploidies: A multicentre prospective cohort trial in Taiwan, Prenatal Diagnosis Song,Y.J., Liu,C.C., Qi,H., et al,(2013) Non invasive prenatal testing of fetal aneuploidies by massively parallel sequencing in a prospective chinese population. Accepted for Prenatal Diagnosis Sparks, A. B., Struble, C. A., Wang, E. T., Song, K., & Oliphant, A. (2012). Noninvasive prenatal detection and selective analysis of cell-free DNA obtained from maternal blood: evaluation for trisomy 21 and trisomy 18. American Journal of Obstetrics and Gynecology, 206(4), 319.e1�C9. Epub 2012 Jan 26.
Wang E, Batey A, Struble C, Musci T, Song K, Oliphant A ,Gestational Age and Maternal Weight Effects on Fetal cfDNA in Maternal Plasma Prenat Diagn. 2013 Apr 2:1-5. Zimmermann,B., Hill,m., et al, Noninvasive prenatal aneuploidy testing of chromosomes 13, 18,21, X, and Y, using targeted sequencing of polymorphic loci. Prenatal Diagnosis 2012, 32, 1�C9
������
���������������������Ļ���֪ͨ������ر�ע��������Դ�ڻ�����������ת�س���������ҽ���������ƴ�ҵ�ߴ��ݸ�����Ϣ���ٽ�ѧ��������ѧϰ֮Ŀ�ģ�������ζ�ű�����ͬ��۵��֤ʵ�����ݵ���ʵ�ԣ�������ҽ�����������ת�ظ��漰��Ȩ�����⣬��������ϵ����Ա�����ǻ����Ը��Ļ�ɾ��������£���֤����Ȩ������ʹ�ñ���վ��Ϣ�ͷ���������ĺ�������������κ����Ρ�
������ҩƷ��Ϣ�����ʸ�֤ ������-��Ӫ��-2010-0046
������ Copyright © 2010www.obstetrics.cn. All Rights Reserved ��ICP��15060573��-14
������������֮���ݽ�����ѧ������Ŀ�ġ����Ӳ������ϻ�ȡ����Ϣ����ֱ��������ϡ����Ƽ��������Ľ������⡣
��վ�������°�Ȩ��ԭ�������У�ת�ؽ�Ϊ������Ϣ�ٽ�ҽѧ��ҵ��չ��������ǵ���Ϊ�ַ�������Ȩ�棬�뼰ʱ��������ϵ�����ǽ����ƴ����ò������ݡ�