无创产前基因检测技术筛查胎儿21三体综合征的效果评价
无创产前基因检测技术筛查胎儿21三体综合征的效果评价
21三体综合征又称唐氏综合征或先天愚型,是一种常染色体疾病。据测算,我国每年将新增唐氏综合征2.3万一2.5万例,每年新出生的唐氏综合征生命周期的总经济负担超过100亿元。目前没有治疗21三体综合征的有效手段,最佳方法是通过产前筛查和产前诊断来进行预防。临床常用的无创产前标志物筛查技术只能帮助判断胎儿患有21三体综合征的风险性,确认胎儿21三体综合征的方法包括羊膜穿刺检查和绒毛膜取样术,但是都属于创伤性方法,会给孕妇和胎儿带来一定的风险。近年来,随着DNA高通量测序技术和生物信息学的发展,出现了多种基因测序技术[1]。本研究客观评价无创产前基因检测技术对于胎儿21三体综合征的筛查效果,为此项技术的临床应用提供证据。
1 资料与方法
1.1 文献筛选标准 纳入标准:①评价无创产前基因检测技术对于胎儿21三体综合征的筛查效果;②结果指标包含无创产前基因检测技术的敏感度和特异度。排除标准:病例报告、主观观点、综述、数据重复发表的文献。
1.2 文献检索策略 检索词包括:DNA、RNA、cffDNA、cffRNA noninvasive prenatal diagnosis、Trisomy、Down syndrome。计算机检索Cochrane Library、PubMed和Embase。检索时间从2000年1月一2013年7月。为提高查全率,追查所有纳入文献的参考文献。
1.3 文献筛选 两名研究者根据纳入与排除标准独立筛选并交叉核对文献。首先阅读文题和摘要,排除明显不符合纳入标准的文献,对可能符合的文献通过阅读全文进行二次筛选,如遇分歧经由第三方评价员商议解决。
1.4 证据质量评价 两名系统评价员独立评价文献质量,并交叉核对,如遇分歧则经讨论或第三方解决。根据《QUADAS一2诊断性试验评价标准(修订版)》对每项纳入研究进行质量评价[2]。
1.5 资料提取方法 设计资料提取表对文献信息进行提取。提取的资料主要包括:文献的基本信息、研究对象的纳入标准、血清基因检测技术的开展时间、待评价的诊断方法、“金标准”诊断方法、真阳性例数、假阳性例数、假阴性例数、真阴性例数、敏感度和特异度等。如果一项研究采用不同的诊断临界值,则提取敏感度和特异度之和最大即准确度最高的诊断学数据。
1.6 数据分析 用Review Manager 5.2软件绘制证据质量评价结果图。数据分析采用Meta Disk 1.4软件,首先探讨多种无创产前基因检测技术筛查胎儿21三体综合征的合并敏感度(pooled sensitivity)、特异度(pooled specificity)、阳性似然比(pooled positive LR)、阴性似然比(pooled negative LR)、合并诊断比值比(pooled diagnostic OR);之后进行异质性分析,如果P<0.05则各纳入研究问存在异质性,通过Meta回归分析观察统计学异质性的来源,并结合纳入研究的特征进行亚组分析。
2 结果
2.1 资料基本信息 检索相关数据库共获取366篇,其中Cochrane Library 19篇、PubMed 260篇、Embase87篇,查重后余345篇,两次筛选后共纳入全文23篇[3-25]。
2.2 纳入文献研究特征 10项研究在美国开展,6项研究在中国开展,4项研究在英国开展。此外,1项研究在荷兰和瑞典开展[7],1项研究由塞浦路斯、希腊和英国的研究者共同完成[24],1项研究在韩国开展[25]。1项研究的研究对象是多胎妊娠,其余22项研究纳入单胎妊娠的孕妇[10]。18项研究仅纳入妊娠早期和中期的研究对象,5项研究纳入了妊娠早、中、晚期的研究对象。6项研究采用选定区域数字化分析技术(digital analysis of selected regions,DAN―SR),8项研究采用大规模平行测序(massively parallel sequencing,MPS),6项研究采用单核苷酸多态性(single nucleotide polymorphism,SNP)等位基因比率分析法,其余3项研究分别采用实时定量PCR(quantitative real―time PCR,qPCR)、甲基化DNA免疫沉淀(methylated DNA immunoprecipitation,Me―DIP)联合qPCR、甲基化特异性定量PCR (quantitative methylation ― specific polymerase chain reaction,qMSP)。21三体综合征确诊的金标准均选用胎儿染色体核型分析,其中1项研究采用原位免疫荧光杂交技术(fluorescent in situ hybridization,FISH)与核型分析[6],另1项研究采用临床诊断与核型分析[17]。
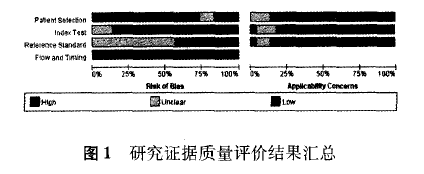
2.3 研究证据的质量评价 纳入研究证据的质量评分中(满分13分),分数最高的是1 1分(1项研究),其次是4项研究1 0分、8项研究9分、4项研究8分、2项研究7分,7分以下有4项研究。质量评价分值(8.74±1.56)分。纳入研究存在的最主要质量问题是证据的偏倚,其中存在高度偏倚的是纳入研究对象、流程和时间,存在不确定偏倚的是“金标准”的选用;证据的适用性相对较好。纳入研究对象评价条目存在的主要问题是研究多采用回顾性设计方案;流程和时间评价条目存在的主要问题是并非所有研究对象均纳人数据分析,即研究存在失访;“金标准”评价条目存在的主要问题是研究并未指出“金标准”结果的判断是否在不知晓待评价的无创产前基因检测结果的情况下进行。见图1。
2.4 Meta分析结果 无创产前基因检测技术对于胎儿21三体综合征的产前筛查具有较高的合并敏感度和合并特异度。见表1
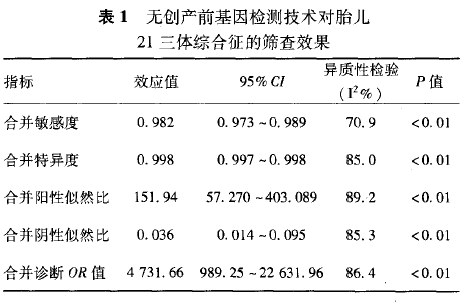
异质性检验发现,合并敏感度、合并特异度、合并阳性似然比、合并阴性似然比、合并诊断OR值的异质性检验结果均提示有异质性存在,因此采用Meta回归探讨异质性的来源。Meta回归结果表明,不同的无创产前基因检测技术与诊断的准确度密切相关(OR=0.10,95%CI:0.04~0.27,P=0.000 1)。
因此,本研究进一步进行了亚组分析,探讨了3种技术即DANSR、MPS和SNP对胎儿21三体综合征的筛查效果。结果表明,筛查胎儿2l三体综合征合并敏感度、合并特异度较高、合并阳性似然比、合并诊断OR值较高的检测技术是DANSR和MPS。见表2。
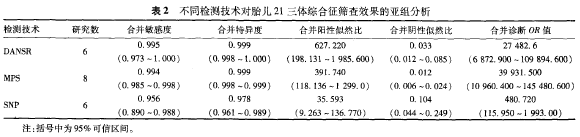
本研究绘制了DANSR和MPS筛查胎儿21三体综合征的合并受试者工作曲线(summary receiver 0perating characteristic curve,SROC),探讨上述两种检测技术的准确性。结果提示,曲线下的面积是0.9991±0.000 3.
3 讨论
胎儿染色体非整倍体异常的无创产前检测是筛查染色体疾病的最新手段,其理论依据是产前血液中存在胎儿游离DNA(cell―free fetal DNA,cffDNA)和胎儿游离RNA(cell―free fetal RNA,cffRNA),胎儿染色体异常会引起游离DNA含量的微量变化。本研究采用卫生技术评估的二次研究方法,通过系统检索无创产前基因检测技术对于胎儿21三体综合征筛查效果的研究文献,提取研究信息,评价研究证据的质量,通过Meta分析方法整合诊断学数据得出客观结论。
本研究发现,常用的筛查胎儿21三体综合征的无创产前基因检测技术包括DANSR、MPS和SNP等位基因比率分析法,也有研究探讨定量PCR的检测价值。l8项研究开展的时问在妊娠早期和中期。纳入分析的研究证据质量评价分值5~11分,平均8.74分,7分及以下的研究共4项。存在的主要质量问题是研究多采用回顾性的设计方案,并非所有研究对象均被纳入数据分析,研究并未指出“金标准”结果的判断是否在不知晓待评价的无创产前基因检测技术的情况下进行。因胎儿染色体异常会引起孕期流产,因此数据缺失问题难以避免。但是,建议研究开展时注意密切随访,尽可能避免其他问题导致的失访。同时建议研究者选用前瞻I生研究设计,并明确指出“金标准”结果的判断人员是否不知晓待评价的研究结果,以提升研究的质量和证据的内部真实性。
为了观察无创产前基因检测技术对胎儿21三体综合征的筛查效果,本文首先分析了各种技术的合并敏感度、合并特异度、合并阳性似然比、合并阴性似然比、合并诊断OR值。似然比不受受试人群中某种疾病发病率的影响,是一个相对独立的、更具有临床意义的诊断性试验效果的评估指标。当阳性似然比>10或阴性似然比<0.1时,确诊某种疾病的可能性显著增加。诊断学OR值将待评价试验的诊断准确度汇总成单一的数值,描述该诊断方法诊断患者时阳性结果的几率是诊断非患者时阳性结果的倍数。根据卫生部产前筛查标准,孕中期无创产前标志物的二联、三联筛查和四联筛查,对唐筛检出率分别大于60%、70%和80%。本研究的Meta分析结果表明无创产前基因检测技术对于胎儿21三体综合征的产前筛查具有较高的检出率。因本文纳入分析的研究包含多种无创产前基因检测技术,而各种技术检测的阈值不尽相同,所以未做阈值分析而是通过Meta回归结合纳入研究的特征探讨异质性来源,此后对同质的资料进行了亚组分析。亚组分析结果和SROC曲线下的面积说明DANSR和MPS具有较高的诊断准确度。本研究结果说明无创产前基因检测技术是胎儿21三体综合征的有效筛查方法。
4 参考文献
1 Chiu RW ,Lo YM.Non―invasive prenatal diagnosis by fetal nucleic acid analysis in maternal plasma:the coming of age [J].Semin Fetal Neonatal Med。2011,16(2):88―93.
2 Whiting PF,Rutjes AW,Westwood ME,et a1.QUADAS一2:a revised tool for the quality assessment of diagnostic accuracy studies[J].Ann Int Med,2011,155(8):529―536.
3 Ashoor G,Syngelaki A,Wagner M,et a1.Chromosome―selective sequencing of maternal plasma cell― free DNA for first―trimester detection of trisomy 21 and trisomy 18 [J]. Am J Obstet Gynecol,2012,206(4):322―325.
4 Nicolaides KH,Syngelaki A,Ashoor G,et a1.Noninvasive prenatal testing for fetal trisomies in a routinely screened first―trimester population [J].Am J Obstet Gynecol,2012,207 (5):374el一374e6.
5 Norton ME,Brar H。Weiss J,et a1.Non―Invasive Chromosomal Evaluation(NICE)study:results of a multicenter prospective cohort study for detection of fetal trisomy 21 and trisomy 18(J].Am J Obstet Gynecol,2012,207 (2):137.
6 Sparks AB,Struble CA,Wang ET,et a1.Noninvasive prenatal detection and selective analysis of ceIl―free DNA obtained from maternal blood:evaluation for trisomy 21 and trisomy 18[J].Am J Obstet Gynecol,2012,206(4):319.
7 Verweij EJ,Jacobsson B,van Scheltema PA,et a1.European Non―Invasive Trisomy Evaluation (EU ―NITE) study:a multicenter prospective cohort study for non―invasive feta1 trisomy 21 testing [J].Prenat Diagn,2013,33 (10):996―1001.
8 Gil MM,Quezada MS,Bregant B,et a1.Implementation of maternal blood cell――free DNA testing in early screening for aneuploidies[J].Obstet Gynecol,2013,42(1):34―40.
9 Bianchi DW ,Platt LD.Goldberg JD,et a1.Genome―wide fetal aneuploidy detection by maternal plasma DNA sequencing[J].Obstet Gynecol,2012,119(5):890―901.
10 Canick JA,Kloza EM, Lambert― Messerlian GM,et a1.DNA sequencing of maternal plasma to identify Down syndrome and other trisomies in multiple gestations[J].Prenat Diagn,2012,32 (8):730―734.
11 Chiu RW . Akolekar R. Zheng YW , et a1.Non ―invasive prenatal assessment of trisomy 21 by multiplexed maternal plasma DNA sequencing:large scale validity study(J]。BMJ,2011,342:c7401.
12 Dan S,Wang W ,Ren J,et a1.Clinical application of massively parallel sequencing―based prenatal noninvasive fetal trisomy test for trisomies 21 and 18 in 1 1, 105 pregnancies with mixed risk factors[J] .Prenat Diagn,2012,32(13):1225―1232.
13 Ehrich M .Deciu C。Zwiefelhefer T,et a1.Noninvasive detection of fetal trisomy 2 1 by sequencing of DNA in maternal blood:a study in a clinical setting(J].Am J Obstet Gynecol,2011,204 (3):205.
14 Jiang F,Ren J,Chen F,et a1.Noninvasive Fetal Trisomy (NIFTY)test:an advanced noninvasive prenatal diagnosis methodology for fetal autosomal and sex chromosomal aneuploidies[J].BMC Med Genomics,2012,5:57.
15 Palomaki GE, Kloza EM , Lambert― Messerlian GM , et a1.DNA sequencing of maternal plasma to detect Down syndrome:an international clinical validation study[J].Genet Med,201l,13 (11):913―920.
16 Palomaki GE,Deciu C,Kloza EM,et a1.DNA sequencing of maternal plasma reliably identifies trisomy 1 8 and trisomy 13 as well as Down syndrome:an international collaborative study[J].Genet Med,2012,14(3):296―305.
17 Dhallan R, Guo X,Emche S,et a1.A non―invasive test for prenatal diagnosis based on fetal DNA present in maternal blood:a preliminary study [J] .Lancet,2007,369 (9560):474―481.
18 Ghanta S,Mitchell ME.Ames M,et a1.Non―invasive prenatal detection of trisomy 2 1 using tandem single nucleotide polymorphisms(J].PLoS One,2010,5(10):3184.
19 Deng YH,Yin AH,He Q,et a1.Non―invasive prenatal diagnosis of trisomy 21 by reverse transeriptase multiplex ligation―dependent probe amplification[J].Clin Chem Lab Med,2011,49 (4):641~646.
20 Lo YM,Tsui NB,Chiu RW ,et a1.Plasma placental RNA allelic ratio permits noninvasive prenatal chromosomal aneuploidy detection(J].Nat Med,2007,13(2):218―223.
21 Tsui NB,Akolekar R, Chiu RW ,et a1.Synergy of total PLAC4 RNA concentration and measurement of the RNA single―nucleotide polymorphism allelic ratio for the noninvasive prenatal detection of trisomy 21[J].Clin Chem Lab Med,2010,56 (1):73―81.
22 Li PQ,Zhang J,Fan JH,et a1.Development of noninvasive prenatal diagnosis of trisomy 21 by RT―MLPA with a new set of SNP markers[J].Arch Gynecol Obstet,2014,289(1):67―73.
23 Jorgez CJ,Dang DD,Wapner R,et a1.Elevated levels of total(matemal and feta1)beta―globin DNA in maternal blood from first trimester pregnancies with trisomy 21[J].Hum Reprod Update,2007,22 (8):2267―2272.
24 Papageorgiou EA ,Karagrigoriou A,Tsaliki E,et a1.Fetal―specific DNA methylation ratio perm its noninvasive prenatal diagnosis of trisomy 21[J].Nat Med,2011,17(4):510―513.
25 Lim JH,Kim SY,Park SY,et a1.Non―invasive epigenetic detection of fetal trisomy 21 in first trimester maternal plasma [J].PLoS One,2011,6(11):e27709.
26 Go AT,van Vugt JM,Oudejans CB.Non―invasive anenploidy detection using free fetal DNA and RNA in maternal plasma:recent progress and future possibilities[J].Hum Reprod Update,2011,17 (3):372―382
互联网药品信息服务资格证 (京)-经营性-2010-0046
产科网 Copyright © 2010www.obstetrics.cn. All Rights Reserved 京ICP备15060573号-14
产科网所刊载之内容仅用于学术交流目的。您从产科网上获取的信息不得直接用于诊断、治疗疾病及您的健康问题。
本站所有文章版权归原作者所有,转载仅为传播信息促进医学事业发展,如果我们的行为侵犯了您的权益,请及时与我们联系,我们将妥善处理该部分内容。