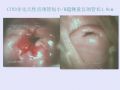
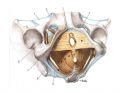
子宫内膜异位症患者卵泡输出率评估卵巢反应性及IVF-ET妊娠结局
卵泡输出率(follicularoutput rate,FORT)最早由Genro等[1]2011年提出,将其定义为B 超监测下hCG日16~22mm排卵前卵泡数(preovulatory follicle count,PFC)与自然月经周期第3d(D3)3~8 mm 窦卵泡数(antrum ovarian count,AFC)的比值,也即FORT=(16~22 mm)PFC×100/(3~8 mm)AFC。最新的观点认为,FORT 是研究卵巢反应性的有力工具。本文回顾性分析子宫内膜异位症(endometriosis,EMs)患者采用225 IU的促性腺激素(gonadotropins,Gn)启动量实施体外受精-胚胎移植(in vitro fertilization-embryotransfer,IVF-ET)助孕,探讨EMs 患者FORT与卵巢反应性及IVF-ET妊娠结局的关系。
资料与方法
一研究对象
回顾性分析2012年1月至2013年11月在南京军区福州总医院妇产科生殖中心行IVET 的239 例EMs 不孕患者,月经来潮第3 天计数窦卵泡(AFC)、hCG 治疗日B超计数排卵前卵泡数(PFC),计算出卵泡输出率(FORT),分析FORT与各项指标的关系。239例EMs 患者按FORT大小排序,分高、低两组,120 例为高FORT组,FORT平均值为(84.75±9.77);119 例为低FORT组,FORT 平均值为(56.62±11.40)。本研究经过福州总医院医学伦理委员会批准,患者均签署了知情同意书。
二EMs 的诊断标准、纳入标准和排除标准
1.纳入标准:①经腹腔镜手术所见证实盆腔子宫内膜紫蓝色异位结节,单纯行子宫内膜异位灶电灼术并行输卵管通液术证实输卵管通畅的EMs患者监测卵泡指导同房试孕半年未孕行IVF-ET治疗;②育龄妇女,月经规则;③年龄≤38岁;④基础FSH(bFSH)≤ 10.0 mIU/ml;⑤首次接受IVF-ET 助孕;⑥移植2 枚新鲜优质胚胎(若患者有且仅有一个优胚,移植1 个);⑦至少3个月未接受雌激素类药物;⑧ Gn 用225 IU 启动量。
2.排除标准:排除卵巢内膜异位症手术史,排除近年内有盆腹腔手术者对卵巢结构及功能有影响而影响排卵质量及妊娠结局的子宫内膜异位症患者。
三、超促排卵方案
黄体中期长方案:于上一周期的第21天按体重注射长效达菲林1.25~1.88mg,14d后查FSH、LH、E2、P,垂体达降调节标准(FSH <5mIU/ml,LH<5 mIU/ml,雌二醇E2 <30 pg/ml,子宫内膜厚度<5 mm),根据患者年龄、基础内分泌和窦卵泡数(AFC)、BMI 等Gn促排卵,包括:果纳芬或HMG,阴超监测卵泡数量、大小及子宫内膜厚度,测E2、P、LH,调整Gn用量,当3个主导卵泡直径>17mm 时,当晚注射hCG 250μg。35~36h后取卵,取卵后当日雪诺酮和地屈孕酮黄体支持。取卵后第3 日移植1~2 枚8- 细胞胚胎。
四、优质胚胎及妊娠结局判定
优质胚胎为2PN来源,碎片<20%,7-细胞以上的胚胎。取卵后72h在阴道B超引导下行胚胎移植。移植14d抽血查hCG,移植28d后B超检查,见妊娠囊及胎心搏动,判定为临床妊娠。移植日若出现宫腔积液、内膜厚度<7 mm、E2>5000 pg/ml 和获卵数>15个这四项条件其中一项者则取消移植。
五、统计学处理
所有资料使用SPSS16.0统计软件进行统计学分析。计量资料采用均数±标准差(x±s),计数资料采用率(%)表示,组间比较采用t检验或X2检验。P<0.05认为差异有统计学意义。
结果
一、EMS患者高FORT与低FORT组一般资料的比较
两组间年龄、不孕年限、体质指数、基础FSH、Gn 用量等差异无统计学意义(P>0.05);基础FSH、HCG日E2值、PFC差异有有统计学意义(P<0.05),见表1。
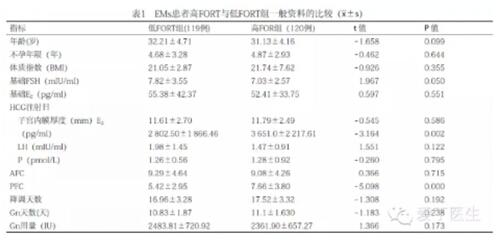
二、EMS患者高FORT与低FORT组卵巢反应性与妊娠结局比较
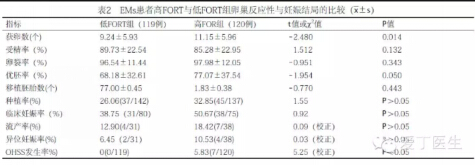
两组间获卵数、优胚率、卵巢过度刺激综合征(ovarian hyperstimulation syndrome,OHSS)发生率差异有统计学意义(P<0.05);其余各项指标差异无统计学意义(P>0.05),见表2。
讨论
获得更多的成熟卵子和可移植优质胚胎以及子宫内膜良好容受性是IVF-ET 成功的必备条件。目前生殖医学研究热点之一是获得客观、准确的指标用于评价卵巢反应性,采取个体化治疗原则制定促排卵方案,提高抱婴率并降低OHSS风险以获得更好的妊娠结局。
过去人们常用体征(包括年龄、身高、BMI等)、激素水平(基础内分泌、抗苗勒管激素(anti mullerianhormone,AMH)[2-3]、hCG日血清E2)和超声评估如窦卵泡数(AFC)[4-5] 等评估卵巢反应性并预测IVF结局,其中年龄、AFC与AMH被认为是最接近理想的指标,但以上指标各有优势,但均是对某个阶段的独立指标进行分析,故不可避免地存在局限性。近年来研究发现在月经周期规律的患者中,卵泡输出率(FORT)可作为评估卵巢反应性及预测IVF-ET 妊娠结局的指标[6-11]。EMs全程影响从排卵、受精、着床到胚胎发育等生殖的全过程[12]。Mekaru 等[13] 发现Ⅰ、Ⅱ期EMs 患者IVF-ET Gn 用量增加、优胚率、妊娠率及活产率均降低。Grzechocinska 等[14] 发现Ⅲ、Ⅳ期EMs 患者妊娠率低于输卵管因素。Singh 等[15] 发现EMs 患者获卵数和受精率降低。盛青菁等[16] 发现,EMs组Gn 用量高于输卵管因素组,hCG 日E2 水平、获卵数、优胚率明显低于对照组。Akihisa等[17]发现EMs 患者超长方案可降低细胞毒性细胞因子和氧化应激的不利影响,种植率和妊娠率高于长方案组。
我们通过EMs 患者卵泡输出率(FORT)评估卵巢反应性及IVF-ET 妊娠结局。邢俊等[18] 推荐Gn使用225 IU启动量使结果更具可比性,我们对EMs 患者也选择Gn用225IU启动量进行研究。本研究的结果显示,EMs患者高、低FORT 两组年龄、不孕年限、BMI、基础E2、Gn用量差异无统计学意义,这些指标与卵巢反应性和妊娠结局均有关,只有这些指标没有差异性才说明后续的两组间卵巢反应性和妊娠结局具有可比性。冷金花等[12]研究发现AFC 在高FORT组最低,在低FORT组最高。我们的研究显示EMs患者高、低FORT两组AFC差异无统计学意义(P>0.05);EMs 患者PFC、hCG日E2、获卵数及优胚率在高FORT组高于低FORT 组,差异有统计学意义,这与邢俊等[18]和Farhi 等[19] 的结果一致;本研究还显示高FORT组EMs 患者有较高的种植率和临床妊娠率,但差异无统计学意义,邢俊等[18] 研究胚胎种植率及临床妊娠率亦有统计学差异,在高FORT组最高,后期我们将要加大样本量进一步研究。Gallot 等[11] 也认为FORT与优胚率呈显著正相关,但他认为受精率并不随着FORT 值的升高而增加,我们的结果与之符合,我们发现在低FORT 值患者中,可表现出更高的受精率。EMs高FORT组流产率和异位妊娠率较低FORT增高,但差异无统计学意义(P>0.05),但OHSS 发生率增高有统计学意义(P<0.05),因此我们注意在促排时要采取个体化方案尽量避免OHSS并发症的发生。
本研究的结果提示,FORT 不受年龄、基础FSH、AFC、基础E2这些常规评价卵巢反应性的因素的影响,是一个独立的指标,既往认为发育至成熟阶段的卵泡数、直径>14 mm的卵泡数或回收卵子数≤3~4个的患者诊断为“卵巢反应不良”,而使用FORT来评价却是不一样的结论,例如某患者的基础窦卵泡数(3~8 mm)为4个,发育成熟的卵泡数为3 个,FORT = 75%,并不能诊断为卵巢反应不良,这种预测能力不受卵泡大小和回收卵子个数的影响[18]。本研究结果认为EMs患者高FORT组具有更好的卵巢反应性,对外源性Gn反应良好、获卵数更多、优胚率、种植率和临床妊娠率更高,妊娠结局更好。FORT是EMs患者IVF-ET 中评价卵巢反应性、指导临床治疗个体化超促排卵方案、剂量制定的更客观的临床指标,可减少卵巢过度刺激或卵巢低反应而取消治疗周期的发生率,达到改善IVF-ET 临床结局的目的,具有广阔的应用前景。
参考文献
[1]Genro VK,GrynbergM,Seheffer JB,et al. Serumantimullerian hormone levels are negatively related to follicular output rate(FORT)in normo-cycling women undergoingcontrolled ovarian hyperstimulation.Hum Reprod,2011,26:671-677.
[2]Bonilla MF,CastilloJC,Caballero O. Predicting ovarian reserve andreproductive outcome using antimüllerian hormone(AMH)and antral follicle count(AFC)in patients with previous assisted reproduction technique(ART)failure. Clin Exp Obstet Gynecol,2012,39:13-18.
[3]Hossein G,ArabzadehS,Hossein RB,et al. Relationsbetween steroids and AMH:impact of basal andintrafollicular steroids to AMH ratios on oocyte yield and maturation rate in womenwith or without polycystic ovary undergoing in vitro fertilization. GynecolEndocrinol,2012,28:413-417.
[4]Rodriguez PJ,CoroleuB,Tur R,et al. Endometriosisand IVF:are agonists really better? Analysis of 1180cycles with the propensity score matching. Gynecol Endocrinol,2013,29:859-862.
[5]Tsakos E,Tolikas A,Daniilidis A,et al. Predictive value of anti-müllerian hormone,follicle-stimulating hormoneand antral follicle count on the outcome of ovarian stimulation in women followingGnRH-antagonist protocol for IVF/ET. Arch Gynecol Obstet,2014,290:1249-1253
[6]Gallot V,BerwangerAL,Genre V,et a1.Antralfollicle responsiveness to follicle-stimulating hormone administration assessedby the follieular output rate(FORT)may predict in vitro fertilization-embryo transfer outcome. HumReprod,2012,27:1066-1072.
[7]梅巳,徐仙,刘春莲,等.卵泡输出率与体外受精一胚胎移植中卵巢反应性的研究.宁夏医学杂志,2012,34:839-841.
[8] Zhang N,Hao CF,Zhuang LL,et al. Prediction of IVF/ICSI outcomebased on the follicular output rate. Reprod Biomed Online,2013,27:147-153.
[9]唐淮云,汤丽莎.卵泡输出率评估卵巢反应性及预测IVF结局的价值.中国现代医学杂志,2014,24:67-70.
[10]Genro V,Matte U,De CE,et al. Frequent polymorphisms of FSHreceptor do not influence antral follicle responsiveness tofollicle-stimulating hormone administration as assessed by the FollicularOutput RaTe(FORT).J AssistReprod Genet,2012,29:657-663.
[11]Gallot V,BerwangerAL,Genre V,et a1. Antralfollicle responsiveness to follicle-stimulating hormone assessed by the FollicularOutput Rate(FORT)predict invitro fertilizationembryo transferoutcome. Hum Reprod,2012,27:1066-1072.
[12]冷金花,戴毅.子宫内膜异位症诊治热点问题.中国实用妇科与产科杂志,2014,30:17-20.
[13]Mekaru K,Yagi C,Asato K,et al. Effects of earlyendometriosis on IVF-ET outcomes. Front Biosci(Elite ED),2013,1:720-724.
[14]Grzechocinska B,WielgosM. Management of infertility in women with endometriosis. Neuro Endocronol Lett,2012,33:674-679.
[15]Singh N,Lata K,Naha M,et al. Effect of endometriosis on implantationrates when compared to tubal factor in fresh non donor in vitro fertilizationcycles. J Hum Reprod Sci,2014,7:143-147.
[16]盛青菁,潘家坪,滕晓明,等.子宫内膜异位症对体外受精- 胚胎移植结果的影响.同济大学学报(医学版),2014,35:80-84.
[17]Akihisa T,YasuhikoN. A pilot study to search possible mechanisms of ultralonggonadotropin-releasing hormone agonist therapy in IVF-ET patients withendometriosis. Ovarian Res,2014,7:100-107.
[18]邢俊,王俊霞,王玢,等.根据卵泡输出率评估IVF 中卵巢的反应性及结局.南京医科大学学报(自然科学版),2014,34:174-178.
[19] Farhi J,Ben-haroushA,Dresler H,et al. Male factor infertilitylow fertilization rate following ICSI and low number of high-quality embryosare associated with high order recurrent implantation failure in young IVFpatients. Acta Obstet Gynecol Scand,2008,87:76-80.
互联网药品信息服务资格证 (京)-经营性-2010-0046
产科网 Copyright © 2010www.obstetrics.cn. All Rights Reserved 京ICP备15060573号-14
产科网所刊载之内容仅用于学术交流目的。您从产科网上获取的信息不得直接用于诊断、治疗疾病及您的健康问题。
本站所有文章版权归原作者所有,转载仅为传播信息促进医学事业发展,如果我们的行为侵犯了您的权益,请及时与我们联系,我们将妥善处理该部分内容。