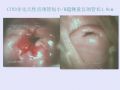
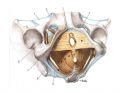
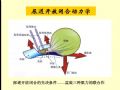
����˫��Ԥ������������ǰ��
����������Ŀǰ��Ϊ������ǰ����̥�ֲ̾�ȱѪ��ȱ���������ڿ�����Ѫ����Ƥ������������-1��sFlt-1���Ϳ�������Ƥ�ǵ��ף�sENG-1����ĸ��Ѫѭ����ء�sFlt-1��sENG-1������Ѫ�����ɹ㷺��Ѫ����Ƥ�������ң��ٴ�����Ϊ��Ѫѹ�Ͷ�ϵͳ�������ˡ������о�������ȱ���յ�����1a��HIF-1a����С��������������Ч����sFlt-1��sENG-1�ķ��ڣ����в���ȷ���Ƿ���������Ӱ�졣����˫�������ڿɰ�ȫʹ�ã�����ͨ��������������Ӵ������Ļ�������HIF-1a��
����Ŀ�ģ�̽����1������˫�Ҷ���sFlt-1��sENG-1���ڵ�Ӱ�죻��2������˫�Ҷ�sFlt-1��sENG-1���ڵ�Ӱ���Ƿ���ͨ��������������Ӵ�������ɣ���3������˫�Ҷ���Ѫ����Ƥ�������ҡ�ĸ��Ѫ�����Ź��ܺ�Ѫ�����ɵ�Ӱ�졣
�����о���ƣ�����ԭ��������֯���й�����ʵ�飬���Զ���˫�Ҷ���̥�̡���Ƥϸ����̥����ë��֯����sFlt-1��sENG-1��Ӱ�졣�����������Ρ������帴�����������ʣ����Զ���˫���Ƿ�ͨ��������������Ӵ�������Ӱ��sFlt-1��sENG-1�ķ��ڡ�������ǰ��������и�̥�̱걾�з���������壬��Ϊʵ����Ͷ����飬�����ö���ѧ��ȷ�������������Ӵ������Ļ��ԡ�
�������ö���˫�ҷ���Ѫ����Ƥϸ����ĸ��ȫѪ�ܣ����о�Ѫ����Ƥ������������������������a��TNF-a������ģ������ʹ����̥������������������ġ��������˶���˫�Ҷ��и���ĤѪ����֯Ѫ�����ɵ�Ӱ�졣
�������������˫�ҿ��Լ���ԭ����Ƥϸ������ëϸ��������ϸ�������������ǰ��̥����ë��֯��sFlt-1��sENG-1�ķ��ڡ��������������Σ�sFlt-1��sENG-1�ķ���������٣���˵������˫�Ҷ�sFlt-1��sENG-1�������ĵ��غܿ�������������ˮƽ��ɵġ����⣬ʹ����������Ӵ��������ͼ�����ͪ�Ϳ�ù�ػ����sFlt-1�ķ��ڣ����һ��˵����sFlt-1�ķ�����ͨ����������ڡ����������ȣ�����ǰ��������и�̥�̵���������Ӵ�����������ǿ��
��������˫�ҿ��Ը���������ǰ����ص���Ƥ�������ҡ�ͬʱ�ɽ���Ѫ����Ƥϸ��Ѫ��ϸ��𤸽����-1��VCAM1����mRNA�ı��VCAM1��TNF-a�յ���������һ����֢ճ�����ӣ���������ǰ����ص���Ƥ�������ҷ���ʱ��������.��ʹ��̥���������������������ƻ��ֻ����Ľ鵼��Ѫ������ЧӦ��������˫�ҿ�����һӰ�졣����˫��ͬʱ���Ը�����sENG-1�鵼��ȫѪ�������ϰ���
�����ܽ����˫�ҿ��Լ���ԭ��������֯��sFlt-1��sENG-1�ķ��ڣ�������ͨ��������������Ӵ�������ɡ�������ǰ��������и�̥���У���������Ӵ������Ļ��Խ���ǿ������˫�ҿ�����Ѫ����Ƥ�������ң��ٽ���Ĥ����Ѫ�����ţ�������Ѫ�����ɡ�����˫�ҿ��ܾ���Ԥ������������ǰ�ڵ�DZ�ܡ�
�������ģ�
��������ǰ����һ�����ص����ﲢ��֢��ÿ��ȫ��Χ���г���100���в�����400��Χ�������ڸü���������ǰ�ڲ������������е���Ҫһ����̥�ֲ̾�ȱѪ��ȱ�����Ӷ����ڿ�����Ѫ����Ƥ������������-1��sFlt-1���Ϳ�������Ƥ�ǵ��ף�sENG-1����ĸ��Ѫѭ����sFlt-1��sENG-1�ķ�����Ѫ����ɹ㷺��Ѫ����Ƥ�������ң���ɶ�����ϵͳ���ˡ�Ŀǰ������Ч�Ʒ�����ֹ�ü����Ľ�չ���ڴ��Ʒ��ͷ����Ծ���Ψһ������ѡ���������һ���������ڿɰ�ȫʹ�õ�ҩ��ȿ��Լ���̥��sFlt-1��sENG-1�ķ��ڣ��ֿ��Ը���Ѫ����Ƥ�������ң���ҩ������ܶ����ƺ�Ԥ������ǰ����Ч��
��������ȱ���յ�����1a��H1F1a�����Ƽ���������ǰ���Ѿ����������ǵĹ㷺��ע��̥��ȱѪȱ��ʱH1F1a���������ӣ���Эͬ�ٽ�sFlt-1�ķ��ڡ���H1F1a�������Խ���sFlt-1�ķ��ڡ�H1F1a����YC-1��G��ë�������Ѿ����ֳ�������̥��sFlt-1�ķ��ڡ����ǣ�YC-1��G��ë��������������ʹ�õİ�ȫ����δ��֪���������ٴ��ж��������Ʒμ��������Ͱ�֢��
���������о���ʾ��Ѱ��һ�ֿ������ڰ�ȫʹ�õ�H1F1a���Ƽ���������˫�ҡ�����˫����һ�ִ�ͳ�Ŀڷ�����Ѫ�ǵ�ҩ����ѱ��������������������������о�����������˫�ҿ�������ֹ���ٰ���ǰ���ٰ�����ɢ�����ӳ���������һ�������������ǶԶ���˫�����ҩ�����ƵĹ�ע��Ҳ���о����ֶ���˫�ҿ���ͨ��������������Ӵ������еĸ������������H1F1a����������裺����˫�ҿ��ܻή�ͻ�����ǰ�ڸ�ŮsFlt-1�ķ��ڡ�
������ǰ�б����ƶ���˫�Ҿ���Ѫ����ѹ�ػ��ԣ����в�ѧ�о�Ҳ��������˫�ҿ�����Ч���Ͷ����ѳ��ۺ����������ߵ���Ѫ�ܲ���֢�����ʡ�������ڶ���˫�ҿ���Ч����Ѫ�ܹ�ǻϸ���е�VCAM-1ˮƽ����Ѫ��ǻ�ڵ�VCAM-1����֢������ǰ��״̬�»����ࡣ�����о����ֶ���˫�һ�̼�������Ѫ�������صķ��ڡ�
����ʵ����Ϻͷ�����
����ʵ����ϣ�������˫��������������֯���й��������飬�������sFlt-1��sENG-1����������������Ӵ�������Ѫ����Ƥ�������ҵ�Ӱ�졣�ֱ�ʹ����̥����֯��Ѫ����֯��
ʵ��ѡ���˶�������̥����֯���������и�̥�̺�������ռ�����������꾲����Ƥϸ����HUVECs����ԭ����ëϸ��������ϸ�������緢������ǰ���ضȵ������и�̥�����ռ�̥����ë��֯����Щ̥�̾�����С��34���ʹ�����������������ϱ�����ACOG�ٴ�ָ�ϡ���ʵ���Һ�������̥����֯��4�������λȡ���걾���л�졣����ȡ̥�̻����и���ͬʱ���и�Ѫѹ�͵�����֢״����������ϱ���24Сʱ���е��״���300mg��̥����ë��֯��ϸ����ǰ������
����Ϊ��������������Ӵ��������ԣ�ѡ��23������һ����緢������ǰ���ضȵ������и���Ϊʵ���飬25�����������Ѫѹ�и���Ϊ�����飬�������и���������ëĤ��Ĥ����������ϲ�֢���������Ϊ����ǰ�ڵ��и������ڵ���������̥�̾������ʹ����������������Ӵ����������о���ϸ��ǰ������
�����ռ������ʹ����и���Ĥ��֯����ǰ����������Ĥ����������������������˫�Ҷ���Ѫ�����ź�Ѫ�����ɵ�Ӱ�졣����ѹ��������Ƿ�����Ѫ�����Ź��ܣ�������Ĥ������֯����������Ѫ�����ɹ��ܡ�
��������ʵ����������˫�ҡ���������Ӵ��������ԡ�sFlt-1��sENG-1��������Ƽ���Ѫ����Ƥ��������
����HUVECs�ܶ�Ϊ24000��ϸ��ÿƽ�����ף����ڵ�2-4��֮�䣬37�棬20�GO2������24Сʱ��ԭ����ëĤ������ϸ���ܶ�Ϊ24000��ϸ��ÿƽ�����ף�������ҹ�Ա�֤���㹻���ϸ�����ڣ���ϴ���������˺ϰ���������Ƭ�κ�����24Сʱֱ���ܶ�Ϊ50000��ϸ��ÿƽ�����ף�37�棬8�GO2������48Сʱ��������sFlt-1��sENG-1�ķ����������Լȡ20mgÿ��������̥����ë��֯37�棬8�GO2������72��Сʱ��
�����ֱ���HUVECs��ԭ����ëĤ������ϸ����̥����ë��֯�м���0��1��2��5mmol/L�Ķ���˫�ң�HUVECs��ԭ����ëĤ������ϸ���м���0��0.5��1mmol/L����˫�Һ�25mmol/Lԭ����ëĤ������ϸ��Ҳ�����ڼ�����������Ӵ��������Ƽ�����ͪ��Ũ�ȷֱ�Ϊ0�� 0.625��1.25��2.5��5 umol/L���Լ���������Ƽ���ù��A��Ũ�ȷֱ�Ϊ 0�� 0.156�� 0.31�� 0.63 ��1.25 umol/L��
�����յ���Ƥ���ܲ��裺��1��ʹ��10ng/ml����������TNF-a����HUVEs����2������25%������̥����ë��֯������������Ĥ��������3����Ĥ�����м���250ng/ml��sFlt-1��37�棬20%O2��ͬʱ��0��1��2��5mmol/L��HUVEs��0��5mmol/L����Ĥ�����м������˫�ң�����3Сʱ����1mmol/L����Ĥ�����м������˫�ң�����120Сʱ��
���� sFlt-1��sENG��VCAM-1��sFlt-1��e15a��i13�IJ���
����ѡ��̥������������������֯��ϸ����ѡ��RNeasy mini�Լ�����ȡRNA���й������飬����HUVECsѪ����Ƥ�����������顣ѡ��DuoSetVEGF R1/Flt-1�Լ��к�DuoSetHuman Endoglin CD/105 ELISA�Լ��н���sFlt-1 ��sENGø���������顣ѡ��NanodropND 1000 �ֹ��ȼƶ�������RNA��ѡ��Applied Biosystems�ĸ�����cDNA��ת¼ø���߰���RNA��ת¼Ϊ����DNA��ѡ��Sybr������������������sFlt-1 e15a��sFlt-1 i13��ѡ��taqman������������������VCAM-1��
������������˫�Ҷ���ϵĤ����Ѫ�����ŵ�Ӱ��
����ѡ��Ѫ��ѹ��ֱ������Բⶨ�Dzⶨ��������ϵĤ����Ѫ�ܡ����м������Ũ�ȵĻ����ģ���0.01 nmol/L ��1umol/L ����ѡ����Ƶ��ɨ�輼������Ѫ�����Ź��ܡ�
����������Ĥ������֯��������˫�Ҷ���Ѫ�����ɹ��ܵ�Ӱ��
����ѡ��calcein AM�Լ��ж���Ĥ������֯��ɫ����40��EVOS FL ���������գ�������Ƭ�еó������
���������
��������˫����Ч����ԭ����Ƥϸ����̥����֯sFlt-1�ķ���
��������sFlt-1��Ҫ����Ƥ��̥����֯���ڣ�����������˫�Ҷ�����Ӱ�졣������HUVECs��Դ����Ƥϸ��������ԭ����ëĤ������ϸ���������м�����������Զ���˫�ң����ή��sFlt-1�ķ��ڡ��������������˫�ң���ֱ����53%��Ƥϸ����63%ԭ��ϸ����sFlt-1�ķ��ڡ�����˫��ͬʱ�ܼ���̥����ë��֯��sFlt-1�ķ��ڣ���Щ̥����ë��֯����4λ���Ϊ����ǰ����С��34��������и���
�������⣬ͬʱ�о��˶���˫�Ҷ������ϸ������̥����ë��֯�в�ͬsFlt-1������mRNA�ı����Ӱ�졣sFlt-1 i13����Ƥϸ���к�����ḻ��sFlt-1�����塣���������Զ���˫�һ������Ƥϸ��sFlt-1 i13mRNA�ı��sFlt-1 e15a������̥����֯����Ҫ�ı����壬����˫�ҿ��Լ���ԭ����ëĤϸ��������ϸ����̥����ë��֯��sFlt-1 e15a��mRNA�ı����Щ��֯���������Ϊ����ǰ����������и�����˿ɵó����ۣ�����˫�ҿ��Խ���sFlt-1�������͵ı��Ҳ�ɽ�����Ƥϸ��/��֯����̥��ϸ��/��֯sFlt-1�ķ��ڡ�
��������˫����Ч����ԭ����Ƥ��̥����֯sENG�ķ���
���������о�����˫�Ҷ���ԭ����Ƥϸ����̥��ϸ��/��֯sENG���ڵ�Ӱ�췢�֣����������Զ���˫�һ���Ч����HUVECs��ԭ����ëĤ������ϸ����sENG�ķ��ڡ�����������ʱ������˫�Ҷ�̥����ë��֯sENG�ķ����н������ƣ����������Ʋ������ԡ���Щ̥����ë��֯�������Ϊ����ǰ����������и���
��������˫��ͨ��������������Ӵ�����������sFlt-1��sENG�ķ���
��������˫��ͨ�������������Զ�������������Ӵ��������ԣ��Ӷ��о�sFlt-1���ڵļ����Ƿ���ͨ��������������Ӵ�������ɵġ����������������帴��������Ҫ��ɳɷ֣��Ƕ���˫�����͵����Ρ�Ҳ����˵���������˫��ͨ�������������Զ�����sFlt-1�ķ��ڣ���ô�������ξͻ�����������������һӰ�졣���ԣ��������ο�����������Ƥϸ����ԭ����ëĤ������ϸ���յ���sFlt-1�ķ��ڵļ��٣���������ͬʱ�����������HUVECs��ԭ����ëĤ������ϸ����sENG�ķ��ڵļ��١���Щ���ݱ���������˫����������Ϊý�����sFlt-1��sENG�ķ��ڡ�
����ͨ��������������Ӵ�����������ԭ����ëĤ������ϸ��sFlt-1�ķ���
����Ŀǰ��������ɵ���sFlt-1���ڵ���һ�۵㻹����ӱ��Ϊ�˵õ������֤�ݣ����о���������������Ӵ��������ͼ��Ƿ��ܼ���sFlt-1�ķ��ڡ�ѡ�������帴��������ͼ�����ͪ�����Լ���ԭ����ëĤ������ϸ��65%��sFlt-1�ķ��ڡ�ѡ�������帴��������ͼ���ù�أ����Լ���75%��sFlt-1�ķ��ڡ�����ͪ�Ϳ�ù�ؼ�����������ϸ�������������о�Ϊ������������sFlt-1�ķ����ṩ�˸���֤�ݡ�
����������ǰ�������̥������������Ӵ��������Ի���ǿ
����������������ֳ���Ӱ��sFlt-1��sENG-1�ķ��ڣ���������������ǰ��̥�̿���ǿ��������Ӵ��������ԡ�23������ǰ���������̥��Ϊʵ���飬25��Ѫѹ�����������̥��Ϊ�����飬�Ƚ϶�����������Ӵ������Ļ��ԵIJ��졣�ó����ۣ�����ǰ���������̥����������Ӵ�������4���������������ǿ�����и�����������ǿ��Ϊ���ԡ����ԣ�������ǰ�������̥������������Ӵ��������Ի���ǿ��
��������˫�һ����Ѫ����Ƥϸ��VCAM-1�ı���
������Ƥϸ��������������Ƥ��֯VCAM-1�ı�����ǿ��ء�VCAM-1���ͷ���Ѫ��ǻ�����ճ�����ӣ����յ�������֢��������ѭ��Ѫϸ��������ǰ�ڻ���Ѫѭ����TNFa������ء�TNFa��һ�ֿ��ϵ�VCAM-1�Ĵ���ϸ�����ӣ�Ϊ�˽������������飺��TNFa����HUVECs�У������ϵ���Ѫ����Ƥϸ��VCAM-1�ı���������˫�Һ�����������TNFa�����VCAM-1�ı����ʾ����˫�ҿ��Զ��ڻ�����Ƥ����������Ӱ�졣
��������˫�һ���ĸ����ĤѪ�ܵ�Ѫ������״̬
����������飬ģ�����շ�ȫѪ�ܹ���������ص�̥�������ͷ���ĸ��ѭ���Ĺ��̡�������Ĥ�����ֱ������̥����������������ͨ�������С���������ͨ�������е�Ѫ�ܼ��뻺���ĺ�100%��������������̥�������������е�Ѫ�ܣ����뻺���ĺ���ֳ�40%�����ˡ���˵�������д��ڵ�̥�����ؿ�������Ѫ�����Ź��ܡ�
��̥����������Ѫ���м������˫�ң�Ѫ�����Ź��ܵ��õ��˻��⡣���Ի�������ص�Ѫ�����Ź��ܵ�Ӱ������ͨ���������
��������˫�ҿɴٽ���ĤѪ����֯ѿ��ʽѪ������
����һ����Ϊ��Ѫ�����ɹ��ܼ������ɵ���̥�ֲ̾�ȱѪ��ȱ������������ǰ�ڽ�һ����չ����̽������˫�һ���Ѫ���������Ƶ������Ƿ���ͨ��sFlt-1�ﵽ������С����������֯ģ���������Ĥ����֯Ѫ���������顣ȡ�ʹ���������Ĥ������֯�걾��������ĤѪ�ܣ������з�ΪС��֯�飬һ����sFlt-1������һ�벻�á�ʵ����Ϊ����sFlt-1��������ĤѪ����֯ѿ��ʽѪ�������������٣����������˫�Һɻ���sFlt-1��Ѫ����֯ѿ��ʽѪ�����ɵ����ơ�
��������
�����о���Ҫ����
��������˫�ҿɽ�����ԭ����֯sFlt-1��sENG�ķ��ڣ�����ƿ�����ͨ��������������Ӵ�������ɵġ���������Ӵ��������������sFlt-1�ķ��ڣ������������ǰ��������Ļ���̥������ǿ��ͨ��ģ������ǰ�ڲ����п��ܴ��ڵ�Ѫ����Ƥ��������״̬�����飬�����˶���˫�ҿ���Ч������Ƥ�������ң�����Ѫ�����Ź��ܣ����ٽ�Ѫ�����ɡ��������������������˫����Ԥ������������ǰ�ڵ�DZ����
������������Ӵ��������������sFlt-1�ķ��ڣ�����˫�ҿ��������ʹ�ͨ·
���������ǵ�һƪ������������Ӵ��������������sFlt-1�ķ��ڡ�ͨ��ʹ�����ֲ�ͬ�����ͼ�������֤��������������������������sFlt-1�ķ��ڡ�
������������ͬʱ���֤���˶���˫��ͨ��������������Ӵ������и��������Զ�������sFlt-1��sENG�ķ��ڡ������������κ�ɻָ��ֶ���˫�������sFlt-1���ڼ��٣����������������ζ�����˫�����sFlt-1�ķ�����Ӱ�졣��������ľ��������ڣ��������α�����ֱ����ΪHIF-1a���ȶ��������Բ�������Ϊֱ��֤��֤�������������帴������ң�����˫�ұ�������Ϊһ��ϸ���ڰ���������Լ�������������ø���������˻��������˫�ҿ�����ͨ����������ϸ�����廯������sFlt-1�ķ��ڡ������ּ�������Ժܵͣ�ԭ�����£�1������˫�Ҷ���Ѫ����Ƥϸ����sFlt-1�ķ�������ͬ��Ӱ�죻2����������̥����ë��֯�й۲쵽��sFlt-1���ڵļ��٣�3��ԭ����ëĤϸ����sFlt-1mRNA���ͣ���˵������˫��ֱ��Ӱ����ϸ����ת¼���ơ�������ȷʵ��δ�����Եر�������˫��һ����ͨ�������������Ӱ���������sFlt-1�ķ��ڡ�
����������ǰ����������ߵ�̥������������Ӵ�����������ǿ
�����о�����������ǰ�����������̥���У���ɵ��Ӵ����������и�������Ծ���ǿ��������ǿ��������Ϊ�����������������ƪ����ר���о���������Ӵ��������ԡ����е�һƪ���������ǵĽ���һ�£�Ҳ�����˸��������Ե�������ǿ������һƪ����ȴ�ó���������Ӵ��������Իή�͵Ľ��ۡ�����ƪ����ֻʹ����12��̥�̱걾��������10������������������о��״�ѡ�����̥�̣��Һ�ǰ��ƪ������������˺ܴ�����������
���о����ݱ���������ǰ��̥������������Ӵ�����������ǿ���������sFlt-1��sENG�ķ��ڡ�
����ͨ��ɸѡ������������Ӵ��������Ƽ�����������������Ե���sFlt-1��sENG�ķ��ڣ�����ܴ���������ǰ��һ���µ�����λ�㡣
��������˫�ҿ���Ѫ����Ƥ�������Ҳ���������ǰ�ڵ�����Ѫ������״̬
����VCAM-1��һ����Ѫ����Ƥ����������ص�������ǰ��ʱ�߱�������Ե��ס���ǰ�о��Ѿ���������˫�ҿ��Լ���Ѫ����Ƥϸ����֢��������ɺͱ������Ѫ��VCAM-1��Ũ�ȡ������������쳣������ǰ��״̬��TNF-a�ı������ǿ��������˫�ҿɼ���Ѫ����Ƥϸ��VCAM-1�ı��
���������о����ֶ���˫�ҿ��滺���ȵ��صֿ�������Ӱ�����Ѫ�ܡ�Ҳ��̥��������������������һ�����о����Ƿ����˫�ҿ�ͬ���滺ĸ��Ѫ�ܡ�ʵ���ϣ�����˫�ҿ����Ѫ�ܶԻ����ĵķ�Ӧ��������Ϊ�������о��ķ������Ա��㷺��������������С��������Ӷ�������״̬��Ѫ�����Ź��ܵ�Ӱ�졣
��������˫�Ҵٽ�Ѫ������
����������ǰ��ʱ��Ѫ�ܴ���һ�ֲ�ƽ��ķ�����״̬��Ϊ����Ƴ�һ������̽������˫�Ҷ�ĸ��Ѫ��Ѫ�����ɵ�Ӱ�졣���⣬�������������ܶ��Ѫ���������顣�絥��ʹ��Ѫ����Ƥϸ�������������飬���ǽ���άĸϸ�����������������������������������顣����Щ�������鲢���籾�о���ѡ����ֶ��������е�ģ������ǰ������ɵ�Ѫ�ܹ������ҡ���Ϊ��Ҫ��������Ѫ�ܣ���Ҫ������Ѫ����Ƥϸ����ƽ����ϸ�����ڵķ�ͬԴ��֯���������о��н���Ƥ�������Һ�sFlt-1������ϵ����һ����ΪsFlt-1�Ǻ�����ǰ�ڽ�����ϵ�ķ��������ӡ��о����֣�sFlt-1��������ĤѪ��������������˫�ҿɻ����������͡����ݱ�������˫�ҿɴٽ�ĸ��Ѫ��������
��������˫�Ҿ���Ԥ������������ǰ�ڵ�DZ��
��������˫�ҿ������ڰ�ȫʹ�ò��Ա�������������������Ȼ������һ��Աȶ���˫�Һ��ȵ��ض���������������Ч����������������У���δ����ͬʱ���и�Ѫѹ��������ǰ�ڵ��и�����ʹ�ö���˫�Һ�����������Ч������˫������3.9%�и�ͬʱ���и�Ѫѹ����5.5%�и�ͬʱ��������ǰ�ڣ��ȵ�������6.2%�и�ͬʱ���и�Ѫѹ����7%�и�ͬʱ��������ǰ�ڡ�����һ����������˫�ҽ��ͷ��ָ�ŮΧ���������ʵ�������������У�Ҳδ��ȷ�������˫��ͬʱ��������ǰ�ڵ�Ӱ�졣����Ҳ������Ϊ�����������߷����Խϵ͡�һ�ݰ��������������ָ���meta�����������˶���˫�Ҷ��ڻ��ж����ѳ��ۺ����и������ֵ�Ӱ�죬����Ҳ��δ����ʹ�ö���˫�Һ�ɽ�������ǰ�ڷ��ա�
����ֵ��ע����ǣ�����Щʵ���У������ڸ�Ѫѹ������ǰ�ڲ�������Ҫ�۲�ָ�ꡣ��������Զ���˫���Ƿ��Ԥ������������ǰ��ѡ����Ȩ�����ٴ��۲�ָ�ꡣ���ĵó��Ľ��ۣ�����˫�ҿɽ���̥��sFlt-1��sENG�ķ��ڲ�������Ƥ�������ң��������Ŷ���˫���ܹ�����̥�̻�ĸ��Ѫ�ܵ�����ǰ��״̬��
��������
������ʵ��ѡ��ԭ��������֯����ǰ�ٴ����飬����������ǰ����������˵�̥���У���������Ӵ�����������ǿ������������Ӵ�����������ëϸ��������ϸ����Ѫ����Ƥϸ��sFlt-1��sENG�ķ��ڡ�����˫�ҿ�ͨ�����������帴�������ԴӶ�����sFlt-1��sENG�ķ��ڡ�ͬʱ������˫�һ�����������ǰ�������Ѫ����Ƥ�������ҵ�һЩ��Ҫ֢״�����ٽ�Ѫ�����ɡ����ԣ�����˫��Ҳ������ΪԤ������������ǰ�����ֶΡ�
�ο����ף�Brownfoot FC, Hastie R, Hannan NJ, Cannon P,Tuohey L, Parry LJ, Senadheera S, Illanes SE, Kaitu'u-Lino TJ, Tong S. Metforminas a prevention and treatment for preeclampsia: effects on soluble fms-liketyrosine kinase 1 and soluble endoglin secretion and endothelial dysfunction. AmJ Obstet Gynecol. 2016 Mar;214(3):356.e1-356.e15. doi:10.1016/j.ajog.2015.12.019. Epub 2015 Dec 22.
������ҩƷ��Ϣ�����ʸ�֤ ������-��Ӫ��-2010-0046
������ Copyright © 2010www.obstetrics.cn. All Rights Reserved ��ICP��15060573��-14
������������֮���ݽ�����ѧ������Ŀ�ġ����Ӳ������ϻ�ȡ����Ϣ����ֱ��������ϡ����Ƽ��������Ľ������⡣
��վ�������°�Ȩ��ԭ�������У�ת�ؽ�Ϊ������Ϣ�ٽ�ҽѧ��ҵ��չ��������ǵ���Ϊ�ַ�������Ȩ�棬�뼰ʱ��������ϵ�����ǽ����ƴ����ò������ݡ�