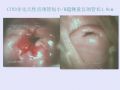
����ǰ�����Ⱦɫ����ͽ���IJ�һ��
1997�꣬����д�ѧ¬�������ڣ�Dannie's Lo����ţ���ѧ�����ˡ��и�Ѫ���ں����൱������ϸ������̥��DNAƬ�Σ�cell-free fetal DNA��cffDNA���������º���ص��о���������ij��֣�����Ϊ��ǰ��ϣ�prenatal diagnosis��ѧ���������ѧ��1�ݡ��������������Ŷ�������nextgenerationsequencing, NGS���������ٷ�չ������ǰ��⣨non-invasive prenatal testing, NIPT����ʽ��Ӧ�����ٴ��ϣ���Ϊ̥��Ⱦɫ���쳣��ǰ��ⷽʽ֮һ��2�ݡ�
��ͳ�ϣ�����̥��Ⱦɫ���쳣�ļ���ַ��������裺��ǰɸ�飨prenatal screening���Ͳ�ǰ��ϡ���ǰɸ�鼴���÷������ԣ�������ʽ�����и�Ѫ��������־��biochemistry markers����⡢̥����������־��飬���г��ڻ������ڶ�̥��Ⱦɫ���쳣���з���������risk assessment��������̥��Ⱦɫ���쳣�߷����и��������ڶ��εIJ�ǰ��ϣ�������Ĥ���̣�amniocentesis������ë������chorionic villus sampling,CVS���������Լ�鷽ʽ������̥��Ⱦɫ����ͣ�karyotype����������ȷ�ϡ�
һ��ɱ����ܵIJ�ǰɸ�����жȣ�sensitivity��ԼΪ85%������ȣ�specificity��Ϊ95%���༴����15%��̥��Ⱦɫ���쳣�����������ó��������ô�ɸ�鷽ʽ���н�5%�ĸ���Ӧ��һ�����ܿ��ܵ� ������abortion������Ⱦ��infection�����յ������Բ�ǰ��ϡ�
NIPT�Է������Է�ʽ���ɼ��и�ѪҺ��Ӧ��NGSֱ�ӷ���Ѫ��������̥�����Ŵ�����DNA�����Ǽ�ӵ�������л��־�������ڳ���̥��Ⱦɫ���쳣����������Ⱦɫ��21������֢��trisomy 21����Ⱦɫ��18������֢��trisomy 18����Ⱦɫ��13������֢��trisomy 13���������жȿɴ�98%���������99%��3-6�ݣ����NIPT���϶�����ȡ����ͳ�ϴӲ�ǰɸ�鵽��ǰ��ϵ�����̥��Ⱦɫ���쳣���ģʽ�����ұ���Ϊ��һ����ϼ���ɸ�졣
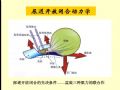
NIPT�Ļ���ԭ��������и�����Ѫ���У���Ҫ�����и�������֯ϸ�����ٲ�������̥��������ϸ������������apoptosis�����γɵIJ�����������DNAƬ�Σ�ƽ��50~200���������NGS�����ڱȶ��Ѿ���������36���Ϊ�������Ӵ�������������� �⣬���ô��ģ���в���massivelyparallel sequencing, MPS����ʽ���б�ʶ��������ű�����ۼƼ��ܣ��������ͬȾɫ��λ����Դ��DNAƬ�γ�����Ŀ��Ƶ�ʣ����ֱ�DNAƬ�������и���̥�̣���������ͳ�Ʒ�ʽ���������ض�Ⱦɫ����Դ��DNAƬ���Ƿ��7�ݡ�����Ŀǰ���ձ鱻ʹ�õķ�����ʽ�ó���Zֵ��Z score������3�������Ⱦɫ��ֵ��normalized chromosomevalues, NCVs������4�����϶�ΪȾɫ��������壨aneuploidy����8�ݡ�
NIPT�е�ϸ������̥��DNAƬ����Ҫ������̥��ϸ�������г��ڣ�̥��һ�γɣ���ëĤĸϸ����trophoblast���Ͳ��ϴ�л�@����DNAƬ��ҲԴԴ���ϵ������и�ѪҺѭ����ϸ������̥��DNAƬ�εİ�˥��ֻ��16 min���и�������2 h����Ҳ�Ҳ����κδ˴λ��е�����̥��DNAƬ�Σ�1�ݡ�����10�ܣ��и�Ѫ����ϸ������DNAƬ�ε�̥����ֵ��fetal fraction��ƽ��Ϊ10.2%��������ÿ��0.11%�ı����������ӣ�ֱ������20�ܣ�̥����ֵ���Խ����Եı���������9�ݡ�һ��ȷ��NIPT��⣬�и�Ѫ����ϸ������DNAƬ�ε�̥����ֵ����Ҫ�ﵽ4%���ϣ�10�ݣ��༴������и�����10�ܼ��ɽ���NIPT��飬����������IJ�ǰɸ����ǰ��ϣ�NIPT���������ڲ�ǰ�������ơ�������������Ӱ���и�Ѫ����ϸ������DNAƬ�ε�̥����ֵ�⣬�и����أ�9-12�ݡ����֣�13�ݡ�Ѫ���־��12-13�ݡ����̣�13�ݡ�Ⱦɫ����ͣ�11,13��Ҳ��Ӱ��̥����ֵ�����أ�Ҳ���ֱ�ӻ��ӵ�Ӱ��NIPT�������жȼ�����ȡ�
���⣬����NIPT������и�Ѫ��̥��ϸ������DNAƬ�ε���Ҫ��Դ��̥�̣������ϣ���һ���Ӧ�������ڲ�ǰ����е���ë���������Ҳ���ܷ�����ͬ����ë������Ⱦɫ����ͼ����ԣ�falsepositive�����棬������ԣ�false negative������Ľ����
����ͳ�ƽ����ʾNIPT�ļ�������ԼΪ0.1%~0.2%��Ȼ����NIPT�����̥��Ⱦɫ����ͽ���IJ�һ�£��ж��ٱ����ɹ����������ʽ��Ⱦɫ�������壨euploidy����Ⱦɫ���������֮������ϵ�ͳ�Ʒ����������ж��ٱ����ɹ�����MPS�������жȵ������ڻ������ϵIJ��죬Ŀǰ�в���֪������̥��Ƕ���ͣ�confined placentalmosaicism��CPM����������Ϊ�ǵ���NIPT�����Ե�ԭ��֮һ��
������̥���д�Լ1%~2%���ֳ�CPM״������һЩ���������У�������ëĤȡ�������ֵ�CPM����Ϊ��NIPT����ļ������йأ�14�ݡ�Mennuti�ȣ�15�����������CPM�йض�NIPT���ΪȾɫ��13������֢�ĸ���������һ��������ֻ����ë������鷢��Ⱦɫ��13������֢����һ������ë�����������46, XX, +13, der ��13,13����q10;q10��������NIPT��������
Hall�ȣ�16�����NIPT�����ʾΪȾɫ��13������֢�ĸ����У���ë�������м��ں�ӫ��ԭλ�Ӻϣ�fluorescence in situ hybridiza��tion, FISH���ʹ�ͳȾɫ����������������Ⱦɫ��13������֢Ƕ���ͣ�47,XY, +13��10��/46,XY������һ����̥������ʱ������������������δ��Ⱦɫ��13������֢������������ѪҺȾɫ����������������ͣ�46, XY��̥��Ⱦɫ���飬�ĸ���ⲿλ��������λ�����쳣����ΪȾɫ��13������֢Ƕ���͡�
��һ����Ȥ�ĸ�����Ⱦɫ�嵥�����壨uni��parentaldisomy, UPD������Ⱦɫ��˫�屣ȫ��disomic rescue�����Ƶ��±���������ͬһ��Ⱦɫ���Դ����˫��֮һ��17�ݡ�һ��NIPT����Ⱦɫ��21������֢�ĸ�������14����ʱ����ë��������QF-PCR���21��Ⱦɫ���ϵ�7���̴����ظ����У�short tandem repeat��STR������ⷢ��������ĸ��Ⱦɫ��21��UPD��������ֹ��̥�̼�ⷢ���ĸ���λ�����һ����Ⱦɫ��21��UPD������������������Ⱦɫ��21������֢�����౨��ָ��CPM������ϲ�̥�������ٻ�����ˣ�һ��NIPT�����ɻ�֤ʵ��һ����ΪCPM����Ӧ�ڲ�ǰ������ϸ��������̥��������������̥������������������������������������������ؼ���������������CPMҲ����ͬʱ����Ⱦɫ�屣ȫ���ƶ�����UPD�龳�������NIPT�������̥��Ⱦɫ����Ͳ�һ��ʱ��UPD����Ҳ��Ӧ�ÿ��ǵ��龳֮һ��
���⣬���ݳ�����NIPT��⣬��ȴδ�ܷ�ӳ�ڴ�ͳȾɫ����ͣ�������֮�����һ��ʱ������оƬ��microarray����⽫�ɽ�һ�����һ�յס�����������Ҫ��Ⱦɫ������֢�⣬������Ⱦɫ��Ҳ���Է���CPM��״������һ����ģ���й���Ⱥ�и��о��У���һ������NIPT��ʾΪ��Ե�Ⱦɫ��������壺47,XXY��Ⱦɫ��21������֢��Ⱦɫ��17������֢��18�ݡ���ë�������д�ͳ��Ⱦɫ������������49, XXX, +7, +21��24��/46, XY����һ��������NIPT�����ʾΪȾɫ��22������֢����������������ѪȾɫ����ͷ��������������Ⱦɫ��22��˫�壬̥��Ⱦɫ����ͷ�������λ����Ⱦɫ��22������֢��������̥����������������������Ⱦɫ���쳣֮���α�����19�ݡ�
������NIPT��̥��Ⱦɫ����ͽ����һ�½��ʱ������Ҫ�����Ƿ�Ϊĸ���������ص���֮Ӱ�졣��һ״������ĸ�屾����Ⱦɫ��������壬��ͨ����������Ⱦɫ���쳣�ϣ������Ƿ������ڻ�����ɸı��״��������ʵ��������solid tumor����20�ݡ�
����ĸ����Ⱦɫ��������壨sex chromo��some aneuploidy, SCA���ĸ��������Ƿ�����һλ25��������и�������NIPT�����ʾΪXȾɫ������֢��21�ݡ���һ������ˮȾɫ����ͷ��������������46,XX���������������Ҳ������������һ�����и�ѪҺȾɫ����ͷ��֣��и�����Ϊ��ȫ��47,XXX���������˵����Ⱦɫ��ķ��������ڱ����������൱���ġ�
��һλ��Ⱦɫ���쳣Ƕ���͵�44��Ů��������NIPT�������ʾXȾɫ����������������˱�������ǰ��һ���������ϵ�45,X֢����֮XȾɫ������������ϣ�18�ݡ���һ�����и�����Ⱦɫ����ͷ����������и�������45,X��3��/46,XX��27�ݡ��������������Ⱦɫ�����������
Wang�ȣ�22�ݷ�չ��һ������MPS��ʽ����Ⱦɫ����ͷ�������ͬʱ�����и���ϸ������������NIPT�����SCA��һ��ʱ���и���Ⱦɫ��Ƕ���͵�״�������181��NIPT���ΪSCA���Ը�������һ��������������16����8.6%���������и�ΪXȾɫ��Ƕ�����쳣���¡��ɴ˿��Ʋ⣬SCA������Ƕ���ͣ���NIPT����пɵ�����̥�������һ���ԣ������ٴ��Ͽ��ܱ����ˡ�Ӧ��NIPT�ж�ΪSCA��Ӧ�ڲ���ǰ�ṩ��ֵ����ۣ����Ժ�����������Ŵ���ѯ��
��һ�����ܲ������ţ�����NIPT�����һ�µ�DNA��Դ��ĸ���ʵ��������20�ݡ�ʵ�ʱ�����İ���������������13������17�ܽ���NIPT��飬�����ʾȾɫ��13������֢��Ⱦɫ��18�ŵ���֢��̥����ˮȾɫ����ͷ�����ʾΪ������46,XY��̥�������������������䣬��һ����̥�̼�鷢��������λ��Ϊ����46,XY���ų���CPM�Ŀ����ԡ������ڲ����������ʹ���ܼ�飬���ֹ���ǻ�ѳ���ת���������ڷ��ڶ���������֮��ȷ��Ϊ��Դ��������Сϸ������small cell carcinoma������֢ϸ����ӫ��ԭλ�Ӻ�Ⱦɫ���֣��ְ�ϸ����80%�����13��Ⱦɫ���ӫ��ǿ�Ƚϵ�18��Ⱦɫ�����ĸߣ�����NIPT�Ľ�������Ŀǰ����������и�������֢ʱ�ж��ٱ������Բ�������NIPT������֣����ٴ�����NIPT���ֶ��Ⱦɫ�������������ʱ����Ӧ����������ԡ�
����NIPT��Ⱦɫ����Ͳ�һ�µ��¼����Խ���ĸ�����Ŀǰ�ٴ����永�����࣬�������ᱨ�ĸ�����ָ�������������崦��������23�ݣ��и�Ѫ����ϸ������DNAƬ�ε�̥����ֵ��10,23�ݣ���Ƕ�����йأ�10�ݡ�Ŀǰ��NIPT���ٴ�������ҵ�����Ʒ�չ���٣��Ѿ���Ϊ����ҽʦ���в�ǰ���ij�����Ŀ֮һ��Ȼ�����ṩNIPT�ļ�ⵥλ��δ��ȫȻ�����ٴ�ҽʦ��������֮NIPT��Ⱦɫ����Ͳ�һ�µ��¼����ԣ��������Խ�������и��������NIPT�����Լ������Ա���Ӧ��ʵ�ʷ����ʸ��ߣ�24�ݡ����⣬NIPT��ⵥλ��δ���ṩ������������������ٴ��ˣ����Իع���������Լ������Ը��������ı���״����δ��NIPT��Ӧ�ö�����ܴ�Ŀǰ�ĸ߷���Ⱥ���ƹ������еĵͷ���Ⱥ������Ԥ���ڴ�һ�龳��NIPT����������ļ�����״���Ʊظ�Ϊ������24��25�ݡ�
���ϼ�ⷽ���ٴ�����ͬ����������ǰ��������¼����ϵͳ���ǿ��еĽ������֮һ��25�ݡ����ɴ˵�¼����ϵͳ�����NIPT���Ը����ȶ�����ǰ�������Ⱦɫ����ͽ���Ƿ�һ�¡�NIPT���Ը��������ٴ�ҽʦ�ṩ֮���ϼ�����ͨ����¼֮��ѯ���ȶ�NIPT������ٴ������һ���ԡ���¼��ϵͳ��������顢�������Խ�¶��NIPT֮�����ʼ������ʡ�����ȷ��֮NIPT�����Ը������ɽ�һ������CPM��UPD������оƬ��⣻ͬʱ����ⵥλ�������ݡ��и�Ѫ����ϸ������DNAƬ�ε�̥����ֵ���в�����������֮�ռ�����һ��̽��NIPT������֮�����������Ը���NIPT���֮���жȼ�����ȡ�
�ο����ף�
��1��Lo YM, Corbetta N, Chamberlain PF, et al.Presence offetal DNA in maternal plasma and serum. Lancet. 1997,350��9076����485-487.
[2��Chiu RW, Lo YM. Clinical applications of maternalplasma fetal DNA analysis:translating the fruits of 15years of research. ClinChem Lab Med. 2013, 51��1����197-204.
��3��Palomaki GE, Deciu C,Kloza EM, et al. DNA sequencingof maternal plasma reliably identifies trisomy 18 andtrisomy 13as well as Down syndrome: an internationalcollaborative study.Genet Med.2012,14��3����296-305.
��4��Ashoor G, Syngelaki A, Wagner M, et al. Chromosome-se-lective sequencing of maternal plasma cell-free DNA forfirst-trimester detection of trisomy21and trisomy18. AmJ Obstet Gynecol.2012,206��4����322. e1-322.e5.
��5��Bianchi DW, Platt LD, Goldberg JD, et al.Genome-widefetal aneuploidy detection by maternal plasma DNAsequencing. Obstet Gynecol.2012,119��5����890-901.
��6��Norton ME, Brar H, Weiss J, et al.Non-invasivechromosomal evaluation ��NICE�� study: results of amulticenter prospective cohort study for detection of fetaltrisomy 21and trisomy18.Am J Obstet Gynecol. 2012,207��2����137.e1-137.e8.
��7��Lo YM, Chan KC, Sun H, et al. Maternal plasma DNAequencing reveals the genome-wide genetic andmutational profile of the fetus. SciTransl Med.2010, 2��61����61ra91.
��8��Fan HC, Quake SR. Sensitivity of noninvasive prenataldetection of fetal aneuploidy from maternal plasma usingshotgun sequencing is limited only by counting statistics.PLoS One2010,5��5���� e10439.
��9��Wang E, Batey A, StrubleC,et al. Gestational age andmaternal weight effects on fetal cell-free DNA in maternalplasma. PrenatDiagn2013,33��7����662-666.
��10��Canick JA, Palomaki GE, Kloza EM, et al. The impact ofmaternal plasma DNA fetal fraction on next generationsequencing tests for common fetal aneuploidies.
����PrenatDiagn2013,33��7����667-674.
��11��Rava RP, Srinivasan A, Sehnert AJ, et al. Circulating fetalcell-free DNA fractions differ in autosomal aneuploidiesand monosomy X.��Epub ahead of print��ClinChem,2013.
��12��Ashoor G, Poon L, Syngelaki A, et al. Fetal fraction inmaternal plasma cell-free DNA at11-13weeks'gestation:effect of maternal and fetal factors. Fetal DiagnTher2012,31��4����237-243.
��13��Ashoor G, Syngelaki A, Poon LC, et al. Fetal fraction inmaternal plasma cell-free DNA at11-13weeks'gestation:relation to maternal and fetal characteristics. Ultrasound ����ObstetGynecol2013,41��1����26-32.
��14��Hahnemann JM, Vejerslev LO. Accuracy of cytogeneticfindings on chorionic villus sampling ��CVS�� diagnosticconsequences of CVS mosaicism and non-mosaicdiscrepancy in centres contributing to EUCROMIC1986-1992. PrenatDiagn1997,17��9����801-820.
��15��Mennuti MT, Cherry AM, Morrissette JJ, et al. Is it timeto sound an alarm about false-positive cell-free DNAtesting for fetal aneuploidy?��Epub ahead of print��Am JObstetGynecol,2013.
��16��Hall AL, Drendel HM, Verbrugge JL, et al. Positive cellfree fetal DNA testing for trisomy13 reveals confinedplacental mosaicism. Genet Med2013,15��9����729-732.
��17��Pan M, Li FT, Li Y, et al. Discordant results between fetalkaryotyping and non-invasive prenatal testing by maternalplasma sequencing in a case of uniparentaldisomy21dueto trisomic rescue. PrenatDiagn2013,33��6����598-601.
��18��Lau TK, Jiang FM, Stevenson RJ, et al. Secondaryfindings from non- invasive prenatal testing for commonfetal aneuploidies by whole genome sequencing as aclinical service. PrenatDiagn2013,33��6����602-608.
��19��Choi H, Lau TK, Jiang FM, et al. Fetal aneuploidyscreening by maternal plasma DNA sequencing:��Falsepositive��due to confined placental mosaicism.PrenatDiagn2013,33��2����198-200.
��20��Osborne CM, Hardisty E, Devers P, et al. Discordantnoninvasive prenatal testing results in a patientsubsequently diagnosed with metastatic disease.PrenatDiagn2013;33��6����609-611.
��21��Yao HL, Zhang L, Zhang H, et al. Noninvasive prenatalgenetic testing for fetal aneuploidy detects maternaltrisomy X. PrenatDiagn2012,32��11����1114-1116.
��22��Wang Y, Chen Y, Tian F, et al. Maternal Mosaicism Is aSignificant Contributor to Discordant Sex ChromosomalAneuploidies Associated with Noninvasive PrenatalTesting.��Epub ahead of print��Clin Chem.2013.
��23��Futch T, Spinosa J, Bhatt S, et al. Initial clinicallaboratory experience in noninvasive prenatal testing forfetal aneuploidy from maternal plasma DNA samples.
����PrenatDiagn2013,33��6����569-574.
��24��Mennuti MT, Cherry AM, Morrissette JJ, et al. Is it timeto sound an alarm about false-positive cell-free DNAtesting for fetal aneuploidy? Am J ObstetGynecol. 2013,
����209��5����415-419.
��25��Cheng PJ, Shaw SW, Noninvasive Prenatal Testing forWhole Fetal Chromosomal Aneuploidies: MulticenterProspective Cohort Trial in Taiwan. Fetal DiagnTher,2014,35��1����13-17.
������ҩƷ��Ϣ�����ʸ�֤ ������-��Ӫ��-2010-0046
������ Copyright © 2010www.obstetrics.cn. All Rights Reserved ��ICP��15060573��-14
������������֮���ݽ�����ѧ������Ŀ�ġ����Ӳ������ϻ�ȡ����Ϣ����ֱ��������ϡ����Ƽ��������Ľ������⡣
��վ�������°�Ȩ��ԭ�������У�ת�ؽ�Ϊ������Ϣ�ٽ�ҽѧ��ҵ��չ��������ǵ���Ϊ�ַ�������Ȩ�棬�뼰ʱ��������ϵ�����ǽ����ƴ����ò������ݡ�