宫腔手术后完全性绒毛膜羊膜分离二例报告并文献复习
绒毛膜羊膜分离(chorioamnioticmembrane separation)是指妊娠14周后胚外体腔消失,羊膜与绒毛膜没有贴附在一起而处于分离状态,超声检查两者之间存在腔隙。根据病因可分为自发性和医源性,自发性绒毛膜羊膜分离病因大多不明确;医源性绒毛膜羊膜分离主要发生于介入性宫内诊断及宫内干预手术后,随着胎儿镜临床应用的日益增多,该问题尤为凸显。绒毛膜羊膜分离临床上较为少见,可导致不良妊娠结局。目前,无临床处理规范和指南可循。浙江大学医学院附属妇产科医院近期收治了两例宫腔手术后发生的绒毛膜羊膜分离患者,现结合文献复习报道如下。
一、临床资料
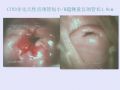
例 1 患者24岁,孕2产0。因停经21周,产前检查发现双胎妊娠并羊水量异常4 d于2013年6月24日入院。患者末次月经2013年1月29日,预产期2013年11月6日。自然受孕,早孕期超声检查提示为单绒毛膜双胎妊娠,停经21周B超检查提示:A胎头位,胎心率136次/分,胎动可及,双顶径5.2 cm,股骨长3.2 cm,前壁胎盘0级,羊水最大平段10 cm,脐动脉收缩期与舒张期血流速度峰值(S/D)比值2.14。A胎心胸比增大,心包腔内见液体深0.5cm,脐带插入腹壁处见2.1 cm×1.1 cm×1.3 cm暗区。B胎头位,胎心率144次/分,胎动可及,双顶径4.5 cm,股骨长2.1 cm,前壁胎盘0级,羊水最大平段1.6 cm,脐动脉S/D比值4.8,静脉导管a波消失。结合B超检查临床诊断为双胎输血综合征(Ⅳ期)。入院后经病情评估并知情同意后,于2013年6月28日在硬膜外阻滞麻醉下行胎儿镜检查+羊膜腔穿刺放液术。术中超声监视下发现胎盘完全位于子宫前壁,分布范围广,在胎盘边缘处穿刺A胎羊膜腔,置入胎儿镜,超声监视发现胎盘边缘处活动性出血,腹壁加压止血5 min后,胎盘出血控制。再次超声检查即发现绒毛膜羊膜分离。羊膜腔穿刺放出淡血性羊水2 000ml。术后第3天再次复查超声,发现A胎绒毛膜羊膜完全分离,羊膜紧密包裹A胎。因考虑胎儿预后不良,患者及家属坚决要求放弃妊娠,予药物注射引产后22 h娩出双胎,体质量分别为320 g和225 g,双胎外观均未见明显畸形。胎盘胎膜自然娩出,羊膜与绒毛膜完全分离,仅在脐带插入处附着于胎盘表面。胎盘表面可见明显血管吻合支。患者产后恢复顺利。
例 2 患者29岁,孕1产0。因停经24周,产前检查发现双胎妊娠并羊水量异常2 d于2014年2月7日入院。末次月经2013年8月17日,预产期2014年5月24日。自然受孕,停经2个多月时B超检查提示为单绒毛膜双胎妊娠。孕24周再次B超检查提示:A胎左前头位,胎心率120次/分,胎动可及,因胎头过低双顶径无法测量,股骨长3.9 cm,腹围20.9 cm,前壁胎盘Ⅰ级,羊水最大平段几乎为0,脐动脉S/D比值部分缺如;B胎右前头位,胎心率136次/分,胎动可及,双顶径6.7 cm,头围23.4 cm,股骨长4.3 cm,腹围19.6 cm,胎盘位于前壁Ⅰ级,羊水最大平段12.3 cm,脐动脉S/D比值2.4。结合B超检查,临床诊断为双胎输血综合征(Ⅲ期)。在病情告知并知情选择后,孕妇及家属均要求放弃胎儿镜治疗,要求终止妊娠。同时因宫腔压力高,孕妇腹部胀痛难以忍受,于2014年2月10日行超声引导下羊膜腔穿刺放液术,在超声监视下,7号穿刺针刺入B胎羊膜腔,抽取羊水,抽吸过程持续约50 min,抽出500 ml色清羊水。同时羊膜腔内注射利凡诺尔100 mg引产,并口服米非司酮50 mg每12小时1次。术后腹胀略好转,当日复查超声发现B胎出现绒毛膜羊膜分离。于2014年2月11日娩出两个女性死胎,体质量分别为770 g及880 g,外观未见明显畸形。羊膜与绒毛膜完全分离,仅在脐带胎盘插入处相连。胎盘表面可见双胎间吻合血管支,B胎胎盘母体面可见6 cm×5 cm血块。
二、讨论
1. 绒毛膜羊膜分离的病因:
根据发病原因,绒毛膜羊膜分离可分为自发性和医源性。由于国内胎儿宫内手术刚处于起步阶段,因此,关于绒毛膜羊膜分离的报道极少,也没有诊治规范可循。Levine等回顾性分析了23883例没有宫腔操作史的孕妇,发现了7例完全性绒毛膜羊膜分离,发生率为1/3400(0.029%)。自发性绒毛膜羊膜分离大部分是完全分离,多数预后不良。由于皮肤、结缔组织与胎膜均起源于外胚层,若胎儿患限制性皮肤病及结缔组织病会常伴有绒毛膜羊膜分离,其发病机制可能与皮肤胶原合成障碍相关。此外,完全性绒毛膜羊膜分离也可能与唐氏综合征相关。医源性绒毛膜羊膜分离根据接受的介入性诊断或干预手术的方式不同,其发生率及严重程度不尽相同:羊膜腔穿刺术后患者绒毛膜羊膜分离发生率为25%,大多为部分性绒毛膜羊膜分离,完全性绒毛膜羊膜分离的发生率仅为0.7%;胎儿镜手术后绒毛膜羊膜分离发生率为20%~50%,完全性绒毛膜羊膜分离发生率为1%;开放性宫内手术绒毛膜羊膜分离发生率高达34%~60%,因开放性手术损伤大,完全性绒毛膜羊膜分离发生率高达10%。宫内操作后发生的绒毛膜羊膜分离的相关高危因素,包括子宫过度膨胀、羊水过多、无法有效抑制子宫收缩等,反复穿刺以及较粗的穿刺针容易导致羊膜的破裂与绒毛膜羊膜分离发也密切相关。本文报道的例1患者发生绒毛膜羊膜分离是在胎儿镜手术后,其胎盘位于前壁,分布广,由于穿刺部位受限,选择在胎盘边缘穿刺。边缘处的绒毛膜羊膜结合较疏松,羊膜腔内高压力的羊水可经过穿刺孔进入绒毛膜羊膜间隙,导致分离。例2患者在羊膜腔穿刺时选择的是普通的7号穿刺针,而不是羊膜腔穿刺专用的22 G穿刺针,针头较后者粗,穿刺抽吸时间长,在宫腔压力高的情况下,羊水也可通过穿刺孔进入绒毛膜羊膜间隙,从而导致分离。
2. 绒毛膜羊膜分离的诊断和鉴别诊断:
发生绒毛膜羊膜分离后,患者无临床症状,部分病例由于继发胎膜早破或胎盘早剥,出现阴道流液或流血,由于临床表现无特异性,超声诊断更具有特殊地位。
(1)超声诊断:绒毛膜羊膜分离的诊断依据为超声检查。理论上讲,妊娠14周前胚外体腔存在,绒毛膜和羊膜生理性分离,妊娠16周后后胚外体腔消失,绒毛膜和羊膜致密粘合。妊娠16周后如超声检查发现可移动的线形强回声羊膜漂浮于羊水中,与绒毛膜分离,分离的羊膜贴附在胎儿躯体,即可诊断为绒毛膜羊膜分离。羊膜完全包裹胎儿,超声检查可见胎儿躯体周围线样强回声,即为完全分离;部分分离表现为羊膜腔内游离线形强回声,局部和绒毛膜结合。
(2)鉴别诊断:绒毛膜羊膜分离需与绒毛膜下出血鉴别,绒毛膜下出血超声图像下表现为绒毛膜处的强回声团块,临床表现上通常有阴道出血,多发生在妊娠早期。而绒毛膜羊膜分离通常和宫腔操作有关,发生在妊娠中晚期,一般无阴道出血,超声图像上为透亮的无回声区。
3. 绒毛膜羊膜分离与妊娠结局:
(1)胎膜破裂自我修复情况:宫内手术破坏了胎膜的完整性,而胎膜自身修复能力低下,羊膜无血管分布,因此,一旦发生绒毛膜羊膜分离,无法自行修复愈合。Gratacós等检查了胎儿镜手术后分娩产妇的胎膜,术后60 d穿刺处破损仍然存在,破损边缘处胎膜细胞的细胞增殖核抗原67、细胞角蛋白(cytokeratin)、波形蛋白(vimentin)表达水平下降,细胞增殖能力极低。提示胎膜损伤后很难通过自身增殖进行修复,随着羊水逐步外渗,可从部分性分离进展到完全性分离。
(2)绒毛膜羊膜分离对胎儿影响:自发性绒毛膜羊膜分离大多数为完全性分离,分离的羊膜可出现羊膜带综合征,包绕胎体或脐带,导致脐带血流受阻、胎儿活动受限,发生胎儿生长受限、胎儿死亡、死产。如果产前诊断通过核型分析或基因检测明确为胎儿染色体异常或限制性皮病,通常预后不良,建议终止妊娠。此外,医源性绒毛膜羊膜分离还增加感染、胎盘早剥、胎膜早破和早产的发生风险。Levine等回顾性分析了25例完全性绒毛膜羊膜分离,只有8例足月分娩,其中1例因脐血管撕裂在阴道分娩时死亡,其余7例都由于脐带压迫,分娩过程中出现胎心监护异常行急诊剖宫产术;其他包括早产儿、宫内死亡、伴羊膜带缠绕等。医源性绒毛膜羊膜分离的不良妊娠结局与分离范围密切相关,开放性宫内手术发生完全性绒毛膜羊膜分离风险最高,羊膜带综合征发生率明显增加,胎死宫内风险高。Adzick等报道了40例因胎儿先天性膈疝行开放性宫内手术,其中5例发生绒毛膜羊膜分离,3例为完全性分离合并羊膜带综合征,1例因脐带受压胎死宫内。Fowler等[6]研究显示,因先天性膈疝行开放性宫内手术导致的绒毛膜羊膜分离的发生率高达60%(21/35),其中合并绒毛膜羊膜炎的发生率为50%,1例因脐带压迫宫内死亡。胎儿镜手术、羊膜腔穿刺、脐带穿刺和绒毛活检等操作主要会造成部分性绒毛膜羊膜分离,目前为止,部分性绒毛膜羊膜分离尚无明确的分级标准,一般认为范围越小预后越好。完全性绒毛膜羊膜分离,其发生快,对胎儿生存威胁极大,因此,一旦出现医源性的完全性绒毛膜羊膜分离,要充分告知孕妇及家属风险,结合孕周,综合评估胎儿预后。需要特别强调的是胎盘早剥问题,本研究中的例2患者,在胎盘娩出后发现胎盘表面有5 cm×6 cm血块,考虑为胎盘早剥,因此在分娩过程中需警惕胎盘早剥,此时超声检查是首选的诊断工具。
(3)绒毛膜羊膜分离的产前检查和分娩问题:发生绒毛膜羊膜分离若选择继续妊娠,需告知孕妇及家属胎儿面临的各项风险,由于胎儿死亡风险高,需住院治疗。每周详细产科超声检查下列项目,包括胎儿生长情况、羊水量、分离范围、羊膜带位置,有无压迫脐带和胎儿肢体。同时,多普勒检查评估有无胎儿窘迫。胎儿电子监护和胎儿生物物理评分有助于评估胎儿宫内情况。若无脐带缠绕受压、胎盘早剥,可选择阴道分娩,分娩期间出现胎心监护异常可考虑急诊剖宫产。
4. 绒毛膜羊膜分离的预防和治疗:
(1)绒毛膜羊膜分离的预防:羊膜腔穿刺发生绒毛膜羊膜分离的发生率达25%,同时,羊膜腔穿刺也是进行最多的宫内诊断操作。Levine等比较了20 G至22 G不同粗细的羊膜腔穿刺针导致绒毛膜羊膜分离发生率的差别,发现穿刺针越细,绒毛膜羊膜分离的发生率越低。Ishikawa等[9]认为直径更细的23 G羊膜腔穿刺针发生绒毛膜羊膜分离的风险更小。所以在羊膜腔穿刺时,选择细针可将绒毛膜羊膜分离发生率降低至0.5%。至于穿刺针型号与抽吸羊水容易度的关系,发现直径更细的23 G羊膜腔穿刺针抽吸羊水的阻力也不大。由于羊膜绒毛膜在妊娠16周前尚未完全闭合,应在妊娠16周后进行羊膜腔穿刺。从本研究中两例患者吸取的经验:在前壁胎盘的胎儿镜手术时,尽量避免胎盘边缘处穿刺,或者在腹腔镜辅助下进行胎儿镜手术。如术前超声评估无法避开该处穿刺,需再充分告知患者及家属绒毛膜羊膜分离的可能性及危害。在选择放弃妊娠的病例,最好选择羊膜腔穿刺专用的22 G或23 G穿刺针,而不是普通的7号穿刺针,穿刺过程中助手协助固定针头,防止反复移动,避免因较粗的穿刺针和长时间穿刺操作导致穿刺孔处撕裂,进而导致绒毛膜羊膜分离。穿刺结束后,进行仔细的超声检查,明确有无绒毛膜羊膜分离发生。
(2)绒毛膜羊膜分离的治疗:Quintero向胎儿镜手术后出现绒毛膜羊膜分离患者的羊膜腔内注入血小板及冷沉淀蛋白,结果发现有5/15的患者绒毛膜羊膜分离消失。胎儿镜手术后使用明胶海绵或胶原制剂,可封闭穿刺位置的胎膜,但不能直接作用在胎膜破裂处,疗效不可靠。丙烯酸酯胶在体外实验中证实可通过黏附破损的胎膜而封补裂口,并能承受较高压力而不发生破裂,是一种较为理想的胎膜修复材料。随着预封闭材料进一步的发展,如能在介入性宫内治疗后完全封闭胎膜破损,即可避免绒毛膜羊膜分离的发生。
随着胎儿医学的发展,各种宫内诊断和宫内手术病例数不断增多,医源性绒毛膜羊膜分离的发生会逐渐增多。医源性绒毛膜羊膜分离可增加术后胎膜早破、早产、羊膜带综合征及胎死宫内的风险。目前,国内最常见的宫内诊断操作是羊膜腔穿刺术,但在术前谈话中的告知手术风险为流产、感染、胎膜破裂等,对绒毛膜羊膜分离的发生及其危害很少告知。术后缺乏有效的超声评估,这也可能是导致国内医源性绒毛膜羊膜分离发生率与国外相差比较大的原因之一。寻找其的病因及防治方法是迫切需要解决的临床问题,定将有助于减少产前诊断及宫内操作、手术后并发症的发生。
互联网药品信息服务资格证 (京)-经营性-2010-0046
产科网 Copyright © 2010www.obstetrics.cn. All Rights Reserved 京ICP备15060573号-14
产科网所刊载之内容仅用于学术交流目的。您从产科网上获取的信息不得直接用于诊断、治疗疾病及您的健康问题。
本站所有文章版权归原作者所有,转载仅为传播信息促进医学事业发展,如果我们的行为侵犯了您的权益,请及时与我们联系,我们将妥善处理该部分内容。